
| A. |  | B. |  | C. |  | D. |  |
分析 A、根据给试管内液体加热的方法分析.
B、根据测定溶液的pH值的方法分析.
C、根据天平的称量范围及注意事项分析.
D、根据稀释浓硫酸的方法分析.
解答 解:A、给试管内的液体加热时,液体的体积不能超过试管容积的$\frac{1}{3}$,故A不正确.
B、测定溶液的pH试纸不能将试纸直接放在待测液中测量,要用玻璃棒蘸取待测液滴在试纸上,故B正确.
C、称量没有腐蚀性的固体药品要放在纸上称量,托盘天平能准确到0.1g,不能称量出12.25g固体;故C不正确.
D、稀释浓硫酸时不能把水倒入浓硫酸中,要将浓硫酸倒入水中,并用琉璃棒搅拌,故D不正确.
故选B.
点评 本题难度不大,熟悉常见仪器的用途和使用时的注意事项;掌握常见实验基本操作的注意事项是解答这类问题的关键.


 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 属于有机物 | B. | 相对分子质量282 | ||
| C. | 一个分子含有44个原子 | D. | 由三种元素组成 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
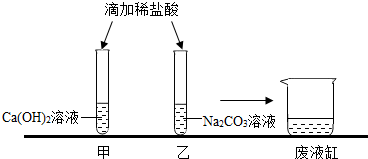 甲、乙同学在学完酸的化学性质后,做了如下实验:
甲、乙同学在学完酸的化学性质后,做了如下实验:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com