
【题目】如图,A—H都是初中化学中常见的物质,常温下,A和B是黑色固体,H为蓝色溶液,F为铁锈的主要成分,它们的转化关系如图所示。请你回答下列问题。
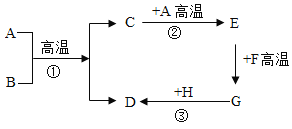
(1)A的化学式为_____,E的一种用途是_____。
(2)反应①的基本反应类型是_____。
(3)写出反应③的化学方程式_____。
【答案】C 冶炼金属或作燃料等 置换反应 
【解析】
由题意常温下,A和B是黑色固体,且二者在高温下能够反应,常温下常见的黑色固体有碳单质、氧化铜、铁粉、四氧化三铁、二氧化锰等,高温下能反应的可以推测单质碳高温下与金属氧化物的反应,例如碳和氧化铜,二者在高温下反应生成铜和二氧化碳;又已知F是铁锈的主要成分,则F是三氧化二铁,高温下与碳单质或一氧化碳可以反应生成铁单质和二氧化碳;H为蓝色溶液,通常情况下含铜离子的溶液为蓝色,G与H反应又生成D,可以推测单质铁与铜离子之间的置换反应生成了铜单质,综上所述,A为碳单质,B为氧化铜,二者在高温下反应生成C二氧化碳和D铜,C二氧化碳和A碳单质高温下反应生成E一氧化碳,E一氧化碳和F三氧化二铁高温下反应生成G铁单质和二氧化碳,G铁单质与H含铜离子的溶液发生置换反应生成D铜单质,经过验证,以上物质推断合理。
(1)A是单质碳,化学式为C,E为一氧化碳,其用途是冶炼金属或作燃料等。
(2)反应①是碳单质与氧化铜在高温下反应生成二氧化碳和铜单质,其基本反应类型是置换反应。
(3)反应③是一氧化碳和三氧化二铁在高温下反应生成铁和二氧化碳,反应的化学方程式为 。
。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】化学兴趣小组的同学走进实验室制备并收集二氧化碳。同学们按下表进行实验,取等质量的大理石分别加入两种不同的酸中(杂质不与酸反应)进行三次实验,产生二氧化碳体积随时间变化曲线如图所示。
实验编号 | 药品 |
Ⅰ | 块状大理石、10% H2SO4溶液 |
Ⅱ | 块状大理石、7% HCl溶液 |
Ⅲ | 大理石粉末、7% HCl溶液 |

(1)图中丙曲线对应实验_______(选填“I”“Ⅱ”或“Ⅲ”)。
(2)小组的同学讨论确定用图中乙曲线对应的药品制备并收集二氧化碳,相应的符号表达式是______________;
(3)不用图中甲曲线对应的药品,理由是______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是初中化学常见的实验或操作,请回答下列问题:
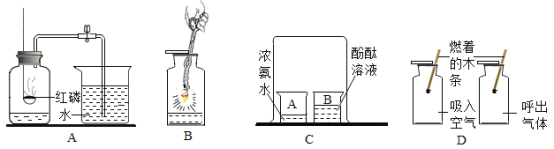
(1)A 实验完毕,进入集气瓶中的水没有达到集气瓶总容积的五分之一,你认为导致这一结果的原因可能是_______。(任写一条)
(2)B实验中集气瓶内放入少量水的目的是________________。
(3)C实验中烧杯 B 中的现象是________________,产生这一现象的原因是________________。
(4)D 实验是探究人体吸入空气和呼出气体成分的实验。实验现象是______________, 由此得出的结论是呼出气体中氧气含量比吸入气体少。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】过碳酸钠(化学式可表示为2Na2CO33H2O2)俗称固体双氧水,极易分解,得到碳酸钠、水和氧气,其化学方程式可表示为2(2Na2CO33H2O2)═4Na2CO3+6H2O+3O2↑。过碳酸钠是很好的消毒剂和供氧剂,广泛应用于洗涤、印染和医药等领域。
通过计算说明:(1)若过碳酸钠分解得到氧气24g,同时产生碳酸钠的质量是多少?
(2)若将上述碳酸钠全部配制成溶质质量分数为10.6%的溶液,需要加入水的质量是多少?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】公交车上备有灭火毡,该灭火毡在无破损的情况下能重复使用。若车内起火,在起火初期快速取出灭火毡,抖开后覆盖在火焰上,直至扑灭。

(1)灭火毡的灭火原理是_____。
(2)请你推测,制造灭火毡的材料应具有_____(答一点即可)等特性。
(3)这种灭火毡我们家庭中也可以备用。若家里的电器起火,使用灭火毡前应先_____,以防止电线绝缘层烧毁而引起电源短路,造成二次火灾。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氢能源是理想能源,氢能源开发一直是前沿科学研究的课题之一。科学家研发出一种以铝镓合金(镓:Ga)和水为原料制取氢气的新工艺,流程如下图所示:
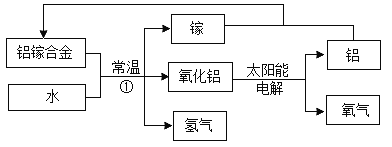
(1)氢气是一种能源,它在空气中燃烧的化学方程式是________________________;氢气被称为“绿色能源”的主要原因是________________________。
(2)反应①中镓的作用是________________________;该反应的化学方程式是________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下面是部分原子或离子的结构示意图.请仔细观察、分析,再回答问题:
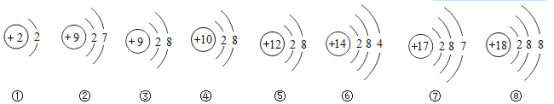
(1)上述粒子中属于阳离子的是_________________;(填序号),属于阴离子的是___________(填序号)。
(2)上述粒子中属于稳定结构的原子是_________________;(填序号).可见,元素的化学性质与原子的________________关系密切。
(3)写出⑤和⑦形成化合物的化学式______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】乙炔(C2H2)是生产聚氯乙烯的重要原料。用电石(主要成分为CaC2)与水反应可制取乙炔,最终还可得到电石渣。某电石渣中含氢氧化钙92.5%,其余为杂质,此电石渣可用于处理电镀厂排出的酸性废水。
(1)乙炔中碳、氢元素的质量比为_____。
(2)100kg上述电石渣中氢氧化钙的质量为_____kg。
(3)已知:CaOH2+H2SO4=CaSO4+2H2O,用上述电石渣处理含硫酸196kg的酸性废水(假设电石渣中的杂质、废水中其他成分均不参加反应),求至少需要电石渣的质量_____(写出计算过程及结果)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在一个密闭容器内有A、B、C、D四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表。下列说法错误的是( )
物质 | A | B | C | D |
反应前质量/g | 4 | 6 | 111 | 4 |
反应后质量/g | 待测 | 6 | 0 | 84 |
A.该闭容器中发生的化学变化属于分解反应
B.反应中B这种物质可能是催化剂
C.该反应中A、C、D四种物质(参加反应或生成)的质量比为35∶111∶80
D.反应后密闭容器中待测A的质量为35 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com