
| A. | 甲醇由碳、氢、氧三种元素组成 | |
| B. | 甲醇中碳、氢、氧三种元素的质量比为3:2:1 | |
| C. | 甲醇由甲醇分子构成 | |
| D. | 一个甲醇分子中共有5个原子 |
分析 A、根据甲醇的化学式进行分析解答;
B、根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,进行解答;
C、甲醇是由分子构成的物质,进行解答;
D、根据 标在元素符号右下角的数字表示一个分子中所含原子的个数,进行解答.
解答 解:A、根据甲醇的化学式CH3OH 可知:甲醇由碳、氢、氧三种元素组成,故A正确;
B、化合物中各元素质量比=各元素的相对原子质量×原子个数之比,所以甲醇中碳、氢、氧三种元素的质量比为12:(1×4):16=3:1:4,故B错误;
C、甲醇是由分子构成的物质,故C正确;
D、根据标在元素符号右下角的数字表示一个分子中所含原子的个数,一个甲醇分子中共有6个原子,故D错误;
故选BD.
点评 本题主要考查化学式的意义、根据化学式确定组成,及一个分子中所含的原子个数等于各元素右下角的数字之和;元素质量等于元素的相对原子质量乘以原子个数;进行解题的能力.


 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:初中化学 来源: 题型:选择题
| A. | 铝合金门窗变暗后用砂纸打磨 | B. | 在铁桶中配制农药波尔多液 | ||
| C. | 尝试用锡来做灯丝 | D. | 切菜刀用后及时冲洗晾干 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 稀盐酸除铁锈,铁锈逐渐消失,溶液逐渐由无色变为黄色 | |
| B. | 纯铁钉放入硝酸银溶液中,铁钉表面有银白色物质析出,溶液由无色逐渐变为浅绿色 | |
| C. | 氢氧化钡溶液和硫酸铜溶液混合,同时产生白色沉淀和蓝色沉淀 | |
| D. | 细铁丝在空气中剧烈燃烧,火星四射,放出大量的热,生成一种黑色固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
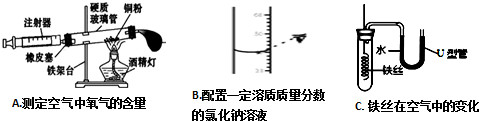
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 偏二甲基肼中元素质量比为C:H:N?1:4:1 | |
| B. | 参加反应的物质中只含C、H、N、O四种元素 | |
| C. | 该反应中N元素的化合价发生改变 | |
| D. | 在宇宙仓中(失重条件下)比地球上难做过滤实验 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
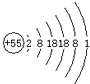 现代工业中,铯铷钨等稀有金属有广泛的用途.我省海洋地质调查研究院在儋州市发现了资源量为大型的铯铷钨矿床.下图为铯(Cs)的原子结构示意图,下列说法不正确的是( )
现代工业中,铯铷钨等稀有金属有广泛的用途.我省海洋地质调查研究院在儋州市发现了资源量为大型的铯铷钨矿床.下图为铯(Cs)的原子结构示意图,下列说法不正确的是( )| A. | 铯属于金属元素 | B. | 铯元素的原子序数是55 | ||
| C. | 铯在化合物中的化合价常为-1价 | D. | 铯原子在反应中易失去电子 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
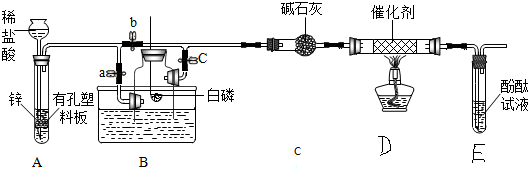
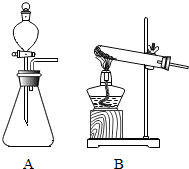
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com