
下列记录的实验现象与事实不相符的是
A. 磷在空气中燃烧产生大量白烟
B. 打开盛有浓盐酸的试剂瓶,看到瓶口有大量白雾
C. 在电解水实验中,正负两极产生的气体体积比约为2︰1
D. 取少量氢氧化钠曝露在空气中,氢氧化钠表面潮湿并逐渐溶解
C 【解析】试题分析:在电解水实验中,正负两极产生的气体体积比约为1:2,C错误。故选C。 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源:洋思中学2018年春学期九年级教学情况化学试卷 题型:科学探究题
实验课上,老师分析金属与盐溶液的反应时指出,在金属活动性顺序表中,排在前面的金属能把位于后面的金属从它的盐溶液中置换出来,但钾、钙、钠等除外。小明很好奇,于是做了金属钠与硫酸铜溶液反应的实验。
【进行实验】取一块绿豆大小的金属钠,放入盛有20毫升硫酸铜溶液的烧杯中,发现金属钠浮在液面上不停打转,产生大量气体,烧杯发烫,溶液中出现了蓝色絮状沉淀,一会儿部分沉淀渐渐变黑,将反应后烧杯中的混合物进行过滤,得滤渣和无色滤液。
【提出问题】①生成的气体是什么?②滤渣的成分是什么?
③无色滤液中的溶质是什么?
【查阅资料】①钠能与水反应生成一种碱,同时放出气体。
②氢氧化铜受热至60~80℃变暗,温度再高分解为相应的金属氧化物和水。
【实验探究一】探究生成的气体是什么?
小明将上述实验药品放入锥形瓶中,立即塞上带导管的单孔塞,将导管通入肥皂水中,将燃着的木条靠近飘起的肥皂泡,有爆鸣声.说明生成的气体是_______,点燃该气体前一定要先______。
【实验探究二】探究滤渣的成分是什么?
【猜想与假设】滤渣中含有Cu(OH)2和________,还可能含有Cu。
【实验验证】
实验步骤 | 实验现象 | 结论 |
取少量滤渣,向其中加入足量的_______ | _______ | 滤渣中没有Cu |
【实验结论】通过实验,小明同学得出结论:钠加入到硫酸铜溶液中会先与水反应,生成物再与硫酸铜反应生成氢氧化铜.请写出生成蓝色沉淀的化学方程式________。
【实验探究三】探究无色滤液的溶质是什么?
【猜想与假设】猜想① Na2SO4 , 猜想②_______。
【实验验证】
实验步骤 | 实验现象 | 结论 |
取少量无色滤液,向其中加入________ | ________ | 猜想①成立 |
【反思与交流】钠加入硫酸铜溶液中出现黑色物质的可能原因是________。
H2 检验纯度 CuO 稀盐酸或稀硫酸 固体全部溶解 CuSO4+2NaOH==Cu(OH)2↓+Na2SO4 Na2SO4和NaOH 无色酚酞试液 不变红(合理答案即可) 钠与水反应放出热量,氢氧化铜受热分解 【解析】(1)该气体点燃时由爆鸣声,说明是氢气,在点燃氢气之前一定要验纯; (2)氢氧化铜受热可能分解生成黑色的氧化铜,故滤渣可能是氢氧化铜、氧化铜和铜的混合物; (3)...查看答案和解析>>
科目:初中化学 来源:湖北省潜江市2017-2018学年度下学期九年级3月月考理科综合化学试卷 题型:填空题
现有生石灰、二氧化锰、铁、水、稀硫酸、苛性钠溶液、硝酸铜溶液、过氧化氢溶液,用以上物质按要求写出化学方程式(物质不能重复使用)
(1)分解反应__________________________________ ;
(2)化合反应__________________________________ ;
(3)置换反应___________________________________;
(4)中和反应___________________________________。
2H2O22H2O+O2↑ CaO+H2O =Ca(OH)2 Fe+2AgNO3=Fe(NO3)2+2Ag 2NaOH+H2SO4=Na2SO4+2H2O 【解析】(1)过氧化氢在二氧化锰作催化剂的条件下分解生成水和氧气,反应方程式为2H2O2 MnO2 2H2O+O2↑; (2)生石灰与水反应生成氢氧化钙,反应方程式为CaO+H2O =Ca(OH)2; (3)铁与硝酸铜...查看答案和解析>>
科目:初中化学 来源:湖北省黄石市2018届九年级3月月考理综化学试卷 题型:实验题
化学实验是学习化学的基础,根据给出的装置回答下列问题:
(1)仪器①的名称是_______________。
(2)实验室用一定质量的氯酸钾制取氧气,通过排水量测定所收集到的氧气体积.
①写出该反应的化学方程式________________________________________;
②若各装置借口的连接顺序是:a→b→c→d,则F装置内的导管(“b”或“c”)延伸方法是____
A.b导管口在液面上方,c导管口在接近瓶底 B.c导管口在液面上方,b导管口在接近瓶底
③根据氯化钾的质量依化学方程式算出的氧气体积为理论值。如果冷却到室温后,实际测得收集到的气体的体积大于理论值(水的体积测量准确)。你认为原因是_______________(写出一点即可)。
④若用加热高锰酸钾的方法制取氧气,装置A有一处不足,请改正___________________,目的是______________________________________。
(3)在上述⑵收集氧气的操作中,使用装置C,加热试管后导管口有气泡冒出,此时导管口还在集气瓶外面,接下来的操作正确的是_____________(填序号)。
①立刻将导管口移入集气瓶 ②等到气泡连续且均匀时,再将导管口移入集气瓶
③立即熄灭酒精灯,将导管口移入集气瓶后在点燃酒精灯。
长颈漏斗 2KClO32KCl+3O2↑ A 试管中的空气进入F装置中 在试管口塞一团棉花 防止高锰酸钾粉末进入导管 ② 【解析】(1)仪器①的名称是长颈漏斗。(2)实验室用一定质量的氯酸钾制取氧气,通过排水量测定所收集到的氧气体积。①该反应的化学方程式是2KClO32KCl+3O2↑;②若各装置借口的连接顺序是:a→b→c→d,则F装置内的导管(“b”或“c”)延伸方法是b导管口在液面上方...查看答案和解析>>
科目:初中化学 来源:湖北省黄石市2018届九年级3月月考理综化学试卷 题型:单选题
要除去下列各组物质中的少量杂质,所选试剂和方法不可行的是( )
选项 | 物质 | 杂质 | 试剂方法 |
A | KCl溶液 | CaCl2 | 加入适量的Na2CO3溶液,过滤 |
B | MnO2 | 炭粉 | 在空气中灼烧 |
C | O2 | 水蒸气 | 通过浓H2SO4洗气 |
D | FeSO4溶液 | CuSO4 | 加入足量铁屑,充分反应后过滤 |
A. A B. B C. C D. D
A 【解析】 选项 物质 杂质 试剂方法 A KCl溶液 CaCl2 加入适量的Na2CO3溶液,生成碳酸钙沉淀和氯化钠,过滤,增添了新的杂质,故A错误; B MnO2 炭粉 在空气中灼烧,碳燃烧生成二氧化碳气体,故B错误; C O2 水蒸气 通过浓H2SO4洗气,浓硫酸具有吸水性,故C正确; ...查看答案和解析>>
科目:初中化学 来源:湖北省黄石市2018届九年级3月月考理综化学试卷 题型:单选题
可用于改良酸性土壤的是______。
A. 小苏打 B. 明矾 C. 纯碱 D. 熟石灰。
D 【解析】改良酸性土壤应是碱性物质,而且价格比较便宜。故选D。 点睛∶熟石灰常用于改良酸性土壤。查看答案和解析>>
科目:初中化学 来源:江苏省无锡市丁蜀学区2018届九年级下学期第一次模拟考试化学试卷 题型:单选题
下图为甲、乙、丙三种固体物质在水中的溶解度曲线,下列说法正确的是
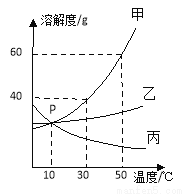
A. 50℃时,分别将等质量的甲和乙溶于适量的水恰好配成饱和溶液,所得溶液的质量前者比后者大
B. 若甲中混有少量的乙,最好采用蒸发结晶的方法提纯甲
C. 将50℃甲、乙、丙三种物质的饱和溶液降温到10℃,析出晶体最多的是甲
D. 向100g 50℃的水中加入65g甲固体,发现全部溶解,一段时间后又有部分甲的晶体析出,可能是因为甲物质溶于水显著放热
D 【解析】A、50℃时,甲的溶解度大于乙的溶解度,分别将等质量的甲和乙溶于适量的水恰好配成饱和溶液,所需要的水甲比乙少,所得溶液的质量前者比后者小,错误;B、甲的溶解度随温度升高变化明显,当甲溶液中混有少量的乙时,可采用降温结晶提纯甲,错误;C、50℃,甲、乙、丙三种物质的饱和溶液降温到10℃时,不知三种溶液质量大小,故无法判断析出晶体质量多少,错误;D、向100g50℃的水中加入65g甲...查看答案和解析>>
科目:初中化学 来源:黑龙江省2018届九年级下学期开学考试化学试卷 题型:实验题
实验室现有氯酸钾、稀盐酸、二氧化锰、大理石、火柴、药匙、镊子及以下仪器:
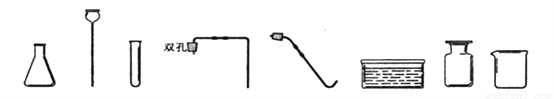
(1)若补充仪器铁架台和____(填名称),并利用上述部分仪器和药品可制取一种气体,则发生反应的化学方程式为_______。
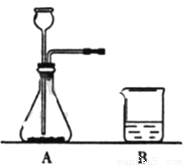
(2)要制备并检验二氧化碳,请连接A、B,并将装置图补充完整________;
(3)B中可观察到的实验现象是_______,这是因为A中大理石与稀盐酸反应生成气体,使A中_____,在压强差的作用下,气体进入B中,产生上述现象。
查看答案和解析>>
科目:初中化学 来源:广东省深圳市2017届九年级三模化学试卷 题型:单选题
下列有关溶液说法,正确的是( )

A. 20℃时,甲、丙溶液的质量分数一定相等
B. 50℃时,甲的饱和溶液的质量分数是33.3%
C. 50℃时,把30g甲放入50g水中能形成80g甲的饱和溶液
D. 只能采用冷却热饱和溶液法获得甲晶体
B 【解析】A、甲,丙不一定是饱和溶液,故溶液质量分数不一定相等,错误;B、50℃时甲溶解度是50g,所以溶液质量是100g水+50g溶质=150g,所以甲的饱和溶液的质量分数是50g÷150g=33.3%,正确;C、50℃时甲的溶解度为50g,所以50g水中只能溶解,25克的甲,所以饱和溶液的质量为75克,错误;D、还可以用蒸发结晶的方法。故选B。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com