
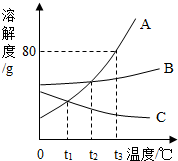
 如图是A、B、C三种固体物质的溶解度曲线图,请结合图示回答下列问题:
如图是A、B、C三种固体物质的溶解度曲线图,请结合图示回答下列问题:

 字词句段篇系列答案
字词句段篇系列答案科目:初中化学 来源: 题型:
| A、氢气在空气中燃烧,生成水 |
| B、黑色的氧化铜粉末与水混合加热后,形成黑色溶液 |
| C、无色的酚酞试液滴入无色的氢氧化钠溶液中,酚酞变蓝 |
| D、铁在氧气里点燃后剧烈燃烧,火星四射,生成黑色固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量溶液于试管中,滴加 |
该溶液是碳酸钠溶液.有关反应的化学方程式为 |
查看答案和解析>>
科目:初中化学 来源: 题型:
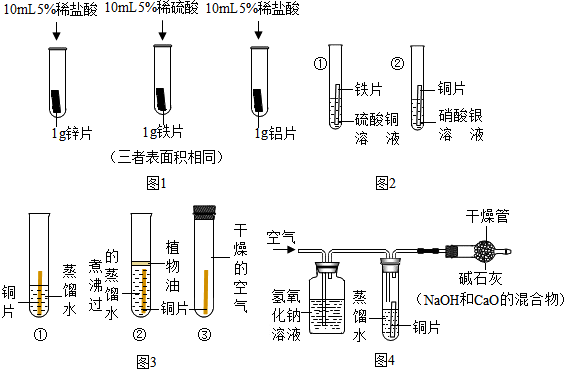
查看答案和解析>>
科目:初中化学 来源: 题型:
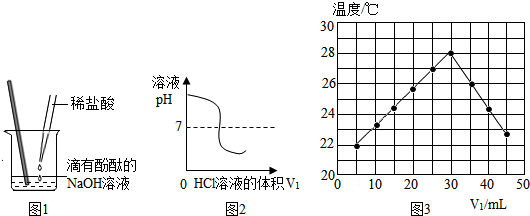
查看答案和解析>>
科目:初中化学 来源: 题型:
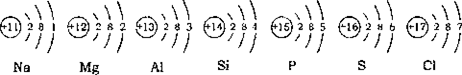
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com