
 ÉÕ±ÖŠÓŠCaCl2ÓėĻ”HClµÄ»ģŗĻČÜŅŗ50g£¬ĻņÉÕ±ÖŠÖš½„¼ÓČė10.0% Na2CO3ČÜŅŗ£¬ĖłµĆČÜŅŗµÄÖŹĮæÓėĖłµĪ¼ÓNa2CO3ČÜŅŗÖŹĮæ¹ŲĻµČēĶ¼£Ø²»æ¼ĀĒÉś³ÉĘųĢåŌŚČÜŅŗÖŠµÄČܽāŗĶĘäĖūĪļÖŹµÄ»Ó·¢£©£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
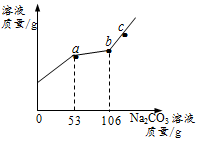
ÉÕ±ÖŠÓŠCaCl2ÓėĻ”HClµÄ»ģŗĻČÜŅŗ50g£¬ĻņÉÕ±ÖŠÖš½„¼ÓČė10.0% Na2CO3ČÜŅŗ£¬ĖłµĆČÜŅŗµÄÖŹĮæÓėĖłµĪ¼ÓNa2CO3ČÜŅŗÖŹĮæ¹ŲĻµČēĶ¼£Ø²»æ¼ĀĒÉś³ÉĘųĢåŌŚČÜŅŗÖŠµÄČܽāŗĶĘäĖūĪļÖŹµÄ»Ó·¢£©£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | a-b¶Ī²śÉśĘųĢå | |
| B£® | cµćČÜŅŗµÄpH£¾7 | |
| C£® | bµćŹ±ÉÕ±ÖŠĪļÖŹµÄ×ÜÖŹĮæĪŖ148.8g | |
| D£® | aµ½b¹ż³ĢÖŠ£¬ČÜŅŗÖŠNaClµÄÖŹĮæ·ÖŹżŌŚ²»¶ĻŌö“ó |
·ÖĪö ĻņÉÕ±ÖŠÖš½„¼ÓČė10.0% Na2CO3ČÜŅŗ£¬Ģ¼ĖįÄĘĻČŗĶĻ”ŃĪĖį·“Ӧɜ³ÉĀČ»ÆÄĘ”¢Ė®ŗĶ¶žŃõ»ÆĢ¼£¬ŗóŗĶĀČ»ÆøĘ·“Ӧɜ³ÉĢ¼ĖįøĘ³ĮµķŗĶĀČ»ÆÄĘ£¬Ņņ“Ė0-a¶ĪŹĒĢ¼ĖįÄĘŗĶĻ”ŃĪĖį·“Ó¦£¬a-b¶ĪŹĒĢ¼ĖįÄĘŗĶĀČ»ÆøĘ·“Ó¦£®
½ā“š ½ā£ŗA”¢a-b¶ĪŹĒĢ¼ĖįÄĘŗĶĀČ»ÆøĘ·“Ó¦£¬²»ÄܲśÉśĘųĢ壬øĆŃ”ĻīĖµ·Ø²»ÕżČ·£»
B”¢cµćČÜŅŗÖŠŗ¬ÓŠĢ¼ĖįÄĘŗĶĀČ»ÆÄĘ£¬ČÜŅŗĻŌ¼īŠŌ£¬ČÜŅŗµÄpH£¾7£¬øĆŃ”ĻīĖµ·ØÕżČ·£»
C”¢ÉčĢ¼ĖįÄĘŗĶĻ”ŃĪĖį·“Ӧɜ³É¶žŃõ»ÆĢ¼ÖŹĮæĪŖx£¬
Na2CO3+2HClØT2NaCl+H2O+CO2”ü£¬
106 44
53g”Į10.0% x
$\frac{106}{53g”Į10.0%}$=$\frac{44}{x}$£¬
x=2.2g£¬
bµćŹ±ÉÕ±ÖŠĪļÖŹµÄ×ÜÖŹĮæĪŖ£ŗ50g+106g-2.2g=153.8g£¬øĆŃ”ĻīĖµ·Ø²»ÕżČ·£»
D”¢Ģ¼ĖįÄĘŗĶĀČ»ÆøĘ·“Ó¦µÄ»Æѧ·½³ĢŹ½¼°ĘäÖŹĮæ¹ŲĻµĪŖ£ŗ
Na2CO3+CaCl2ØTCaCO3”ż+2NaCl£¬
106 100 117
ÓÉŅŌÉĻÖŹĮæ¹ŲĻµæÉÖŖ£¬ĻņÉÕ±ÖŠÖš½„¼ÓČė10.0% Na2CO3ČÜŅŗŹ±£¬ČÜŅŗÖŹĮæŌö¼ÓµÄ²»ČēĀČ»ÆÄĘÖŹĮæŌö¼ÓµÄæģ£¬Ņņ“Ėaµ½b¹ż³ĢÖŠ£¬ČÜŅŗÖŠNaClµÄÖŹĮæ·ÖŹżŌŚ²»¶ĻŌö“ó£¬øĆŃ”ĻīĖµ·ØÕżČ·£®
¹ŹŃ”£ŗBD£®
µćĘĄ ±¾ĢāÖ÷ŅŖæ¼²éĪļÖŹµÄŠŌÖŹ£¬½ā“šŹ±ŅŖøł¾Żø÷ÖÖĪļÖŹµÄŠŌÖŹ£¬½įŗĻø÷·½ĆęĢõ¼ž½ųŠŠ·ÖĪö”¢ÅŠ¶Ļ£¬“Ó¶ųµĆ³öÕżČ·µÄ½įĀŪ£®


 Ļ°Ģā¾«Ń”ĻµĮŠ“š°ø
Ļ°Ģā¾«Ń”ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Õż³£ÓźĖ®Ę«ČõĖįŠŌŌŅņ£ŗSO2+H2OØTH2SO4 | |
| B£® | Éś»īÖŠÓĆĢģČ»Ęų×÷Č¼ĮĻ£ŗC2H3OH+3O2$\frac{\underline{\;µćČ¼\;}}{\;}$2CO2+3H2O | |
| C£® | ÓĆŠ”ĖÕ“ņÖĪĮĘĪøĖį¹ż¶ąÖ¢£ŗNaHCO3+HClØTNaCl+CO2”ü+H2O | |
| D£® | ÓĆĻ”ŃĪĖį³żĢśŠā£ŗ2HCl+FeOØTFeCl2+H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÅäÖĘ15%µÄ¹żŃõŅŅĖįČÜŅŗ100æĖ£¬ŠčŅŖ¹żŃõŅŅĖį15æĖ | |
| B£® | ÅäÖĘŹ±°Ń¹żŃõŅŅĖįµ¹ČėĮæĶ²ÖŠ½Į°čČܽā | |
| C£® | ĮæĶ²ĮæČ”Ė®Ź±£¬Čē¹ūŹÓĻßø©ŹÓ£¬ŌņÅäÖĘČÜÖŹµÄÖŹĮæ·ÖŹżĘ«“ó | |
| D£® | ÅäÖĘŗƵÄČÜŅŗ×°ČėŹŌ¼ĮĘæÖŠ£¬øĒŗĆĘæČū²¢ĢłÉĻ±źĒ© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½«ŹŖŅĀ·žĮĄŌŚĶØ·ēĻņŃō“¦ | B£® | °ŃŠĀĻŹµÄŹß²Ė×°Čė±£ĻŹ“üÖŠ | ||
| C£® | øųŹ¢ÓŠ¾Ę¾«µÄĘæ×Ó¼ÓøĒ | D£® | øų²„ÖÖŗóµÄÅ©Ģļø²øĒµŲĤ |
²éæ““š°øŗĶ½āĪö>>
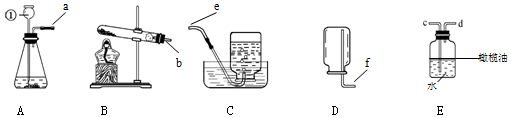
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
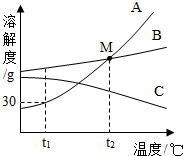 ČēĶ¼ŹĒA”¢B”¢CČżÖÖĪļÖŹµÄČܽā¶ČĒśĻߣ¬¾ŻĶ¼»Ų“š£ŗ
ČēĶ¼ŹĒA”¢B”¢CČżÖÖĪļÖŹµÄČܽā¶ČĒśĻߣ¬¾ŻĶ¼»Ų“š£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŗµŖ | B£® | ±łĖ®»ģŗĻĪļ | ||
| C£® | Ź„ÄĮĢģȻӊ»ś“æÅ£ÄĢ | D£® | ¹āÄÜĖÕ“ņĖ® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢ½¾æĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com