
分析 (1)根据甲烷与水蒸气在高温催化条件下反应写出反应的化学方程式;
(2)根据可燃性的气体与空气的混合气体在点燃时会发生爆炸分析;
(3)根据在该实验过程中需要测定生成的水蒸气的质量分析回答;
(4)根据质量守恒定律分析判断物质的组成;
(5)根据实验的目的、装置的特点分析回答装置的作用
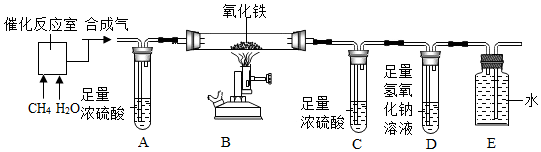
解答 解:(1)由题意可知,甲烷与水蒸气在高温催化条件下反应生成了一氧化碳和氢气,反应的化学方程式 为:CH4+H2O$\frac{\underline{\;催化剂\;}}{高温}$3H2+CO.
(2)由于合成气是可燃性的气体,实验开始前要先通一会“合成气”,然后再点燃B处的酒精喷灯,目的是:排净玻璃管中的空气,防止高温时引起爆炸.
(3)由于在该实验过程中需要测定生成的水蒸气的质量,装置C和D的连接顺序颠倒,会影响实验操作,原因是不能准确地测出生成水的质量;
(4)由A的质量增加,说明了混合气体中含有水蒸气;C装置增加的质量是生成的水的质量,原气体中含有氢元素,且氢元素质量=3.6g×$\frac{2}{18}$×100%=0.4g;D装置增加的质量是反应生成的二氧化碳的质量,且碳元素质量=3.3g×$\frac{12}{44}$×100%=0.9g;甲烷气体中C、H元素质量比=12:(1×4)=3:1,则混合气体中C、H元素质量比=0.9g:0.4g=9:4,因此可判断混合气体中含有甲烷同时含有CO、H2气体,所以,则可推断出该“合成气”的组成物质为:CO、H2O、CH4、H2.
(5)装置A中由浓硫酸,能吸收水分,在实验过程中的作用是除去水蒸气;由E装置的特点可知,E的作用是:收集尾气.
故答为:(1)CH4+H2O$\frac{\underline{\;催化剂\;}}{高温}$3H2+CO;(2)排净玻璃管中的空气,防止高温时引起爆炸:;(3)不能准确地测出生成水的质量;(4)CO、H2O、CH4、H2;(5)除去水蒸气;收集尾气,防止污染空气.
点评 可燃物完全燃烧时,可燃物中的碳元素全部生成二氧化碳,可燃物中的氢元素全部生成水;可燃物完全燃烧生成二氧化碳和水,可判断可燃物中一定含C、H元素.


 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 细铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁 | |
| B. | 硫在空气中燃烧,发出明亮的蓝紫色火焰 | |
| C. | 红磷在空气中燃烧产生大量白烟 | |
| D. | 木炭在氧气中燃烧,发出黄色火焰,生成有刺激性气味的气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 反应属于氧化反应 | |
| B. | X的化学式是Ag2S | |
| C. | 反应前后元素的种类不变 | |
| D. | 反应前后所有元素的化合价都发生了变化 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com