【答案】
分析:(1)①回忆空气的组成:(体积比)氧气21%;,氮气78%,稀有气体0.94%;,二氧化碳0.03%;其他气体和杂质0.03%.
②溶剂是一种可以溶解固体、液体或气体溶质的液体,继而成为溶液.在日常生活中最普遍的溶剂是水.
③一氧化碳是无色、无臭、无味的气体,故易于忽略而致中毒.一氧化碳中毒的原因是因为一氧化碳进入人体之后会和血液中的血红蛋白结合,进而排挤血红蛋白与氧气的结合,从而出现缺氧而中毒.
④掌握碱的定义,即化合物中含有的唯一阴离子氢氧根离子(氨水也能在水溶液中电离出氢氧根离子属碱);
⑤碳酸氢钠俗称“小苏打”白色细小晶体,固体50℃以上开始逐渐分解生成碳酸钠、二氧化碳和水,溶于水时呈现弱碱性.常利用此特性作为食品制作过程中的膨松剂;
(2)根据现有H
2、O
2、H
20、CO、NaHCO
3、NaOH等物质,符合分解反应条件的物质有H
2 0、NaHCO
3写出其反应的化学方程式.
解答:解:(1)①空气的组成:(体积比)氧气21%;,氮气78%,稀有气体0.94%;,二氧化碳0.03%;其他气体和杂质0.03%.故答案为:O
2;
②溶剂是一种可以溶化固体,液体或气体溶质的液体,继而成为溶液.在日常生活中最普遍的溶剂是水.故答案为:H
2 0③一氧化碳中毒的原因是因为一氧化碳进入人体之后会和血液中的血红蛋白结合,进而排挤血红蛋白与氧气的结合,从而出现缺氧,引起中毒.故答案为CO;
④碱是:化合物在水溶液中电离出唯一阴离子氢氧根离子;故答案为:NaOH;
⑤碳酸氢钠俗称“小苏打”白色细小晶体,固体50℃以上开始逐渐分解生成碳酸钠、二氧化碳和水,溶于水时呈现弱碱性.常利用此特性作为食品制作过程中的膨松剂.故答案为:NaHCO
3.
(2)根据现有H
2、O
2、H
20、CO、NaHCO
3、NaOH等物质,符合分解反应条件的化学方程式的有:2NaHCO
3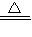
Na
2CO
3+H
2O+CO
2↑2H
2O
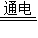
2H
2↑+O
2↑.
故答案为:(1)①O
2;②H
2 0;③CO;④NaOH;⑤NaHCO
3.
(2)2NaHCO
3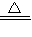
Na
2CO
3+H
2O+CO
2↑;2H
2O
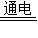
2H
2↑+O
2↑.
点评:此题考查一些常见物质的性质及用途,能判断出题给物质符合发生分解反应的物质,写出其化学方程式,此题能锻炼学生的分析、解决问题的能力,堪为好题.

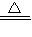 Na2CO3+H2O+CO2↑2H2O
Na2CO3+H2O+CO2↑2H2O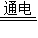 2H2↑+O2↑.
2H2↑+O2↑.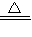 Na2CO3+H2O+CO2↑;2H2O
Na2CO3+H2O+CO2↑;2H2O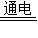 2H2↑+O2↑.
2H2↑+O2↑.
