
分析 (1)稀硫酸和石灰石反应,生成微溶性固体硫酸钙,它覆盖在石灰石表面,使酸与石灰石脱离接触,导致反应太缓慢;
(2)已知条件盐酸溶液和溶质的质量分数然后根据碳酸钙与盐酸反应的化学方程式,即可计算出的该样品中参加反应的碳酸钙质量,根据质量分数=$\frac{碳酸钙质量}{样品的质量}$×100%计算即可.
解答 解:(1)稀硫酸和石灰石反应,有关化学方程式为:CaCO3+H2SO4(稀)═CaSO4+H2O+CO2↑,结果生成微溶性固体硫酸钙,它覆盖在石灰石表面,使酸与石灰石脱离接触,导致反应太缓慢.
(2)设该样品中参加反应的碳酸钙质量为x,生成氯化钙的质量为y,生成二氧化碳的质量为z,
CaCO3 +2HCl═CaCl2 +H2O+CO2↑
100 73
x 73g×10%
$\frac{100}{x}$=$\frac{73}{73g×10%}$,
解之得:x=10g;
该样品中碳酸钙的质量分数=$\frac{10g}{15g}$×100%=66.7%;
故答案为:(1)稀硫酸和石灰石反应,生成微溶性固体硫酸钙,它覆盖在石灰石表面,使酸与石灰石脱离接触,导致反应太缓慢.
(2)66.7%;
点评 本题主要考查学生利用化学方程式和溶质质量分数公式进行计算的能力.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 打开浓HCl的试剂瓶会产生白雾,打开浓硫酸的试剂瓶也会产生白雾 | |
| B. | 氢氧化钠易溶于水,氢氧化钙也易溶于水 | |
| C. | 铁能与稀硫酸反应生成氢气,铜也能与稀硫酸反应生成氢气 | |
| D. | 稀盐酸能使紫色石蕊试液变红色,稀醋酸也能使紫色石蕊试液变红色 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
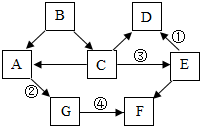 A-G表示初中化学的常规物质,它们之间的转化如图所示(部分反应物、生成物和反应条件已罗去).已知:A、B、C、F均为气体,且C、F可做燃料,D和E为常见金属,且E是世界年产量最高的金属,常温下,G为无色无味液体,请回答下列问题
A-G表示初中化学的常规物质,它们之间的转化如图所示(部分反应物、生成物和反应条件已罗去).已知:A、B、C、F均为气体,且C、F可做燃料,D和E为常见金属,且E是世界年产量最高的金属,常温下,G为无色无味液体,请回答下列问题查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
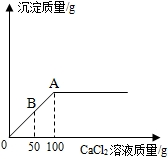 (1)小丽想测定某瓶部分变质的NaOH溶液中 Na2CO3的质量分数.现取20g待测溶液,向其中逐滴加入1.11%的CaCl2溶液,产生沉淀质量与所加CaCl2溶液质量的关系如图所示:
(1)小丽想测定某瓶部分变质的NaOH溶液中 Na2CO3的质量分数.现取20g待测溶液,向其中逐滴加入1.11%的CaCl2溶液,产生沉淀质量与所加CaCl2溶液质量的关系如图所示:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 长期饮用白开水 | B. | 用甲醛溶液浸泡海鲜 | ||
| C. | 食品袋里充入氮气延长食品保质期 | D. | 食用蔬菜以补充维生素 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
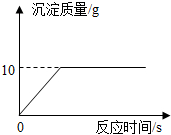 某学校兴趣小组的同学,为测定实验室中一瓶标签破损的碳酸钠溶液中溶质的质量分数,取该碳酸钠溶液20g,向其中加入22g的氢氧化钙溶液,恰好完全反应,生成的沉淀质量与反应时间的关系如图所示,请你据此分析:
某学校兴趣小组的同学,为测定实验室中一瓶标签破损的碳酸钠溶液中溶质的质量分数,取该碳酸钠溶液20g,向其中加入22g的氢氧化钙溶液,恰好完全反应,生成的沉淀质量与反应时间的关系如图所示,请你据此分析:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com