

分析 (1)根据硫酸铁和铁反应生成硫酸亚铁进行分析;
(2)根据溶液甲中的溶质为Fe2(SO4)3、CuSO4及H2SO4,铁和硫酸铜反应生成硫酸亚铁和铜进行分析;
(3)根据铁锈和硫酸反应生成硫酸铁和水,硫酸铁和铁会生成硫酸亚铁进行分析;
(4)根据碳酸亚铁是沉淀,硫酸亚铁经过步骤Ⅱ生成了碳酸亚铁,所以该试剂可以是碳酸钠进行分析;
(5)根据不溶物中含有置换出的铜和反应剩余的铁进行分析.
解答 解:(1)硫酸铁和铁反应生成硫酸亚铁,化学方程式为:Fe2(SO4)3+Fe=3FeSO4;
(2)溶液甲中含有硫酸铜,硫酸铜和加入的铁屑反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4=Cu+FeSO4;
(3)步骤Ⅰ中,废铁屑含有少量铁锈,对产物的成分没有影响,原因是铁锈与硫酸反应生成硫酸铁,硫酸铁和铁会生成硫酸亚铁;
(4)碳酸亚铁是沉淀,硫酸亚铁经过步骤Ⅱ生成了碳酸亚铁,所以该试剂可以是碳酸钠;
(5)通过推导可知,不溶物中含有置换出的铜和反应剩余的铁,所以步骤Ⅲ回收铜的方法为:加入过量的稀硫酸,过滤、洗涤、干燥.
故答案为:(1)Fe2(SO4)3+Fe=3FeSO4;
(2)Fe+CuSO4=Cu+FeSO4;
(3)铁锈与硫酸反应生成硫酸铁,硫酸铁和铁会生成硫酸亚铁;
(4)碳酸钠;
(5)加入过量的稀硫酸,过滤、洗涤、干燥.
点评 在解此类题时,首先分析题中考查的问题,然后结合学过的知识和题中所给的知识进行解答.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:实验探究题
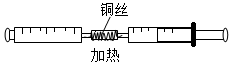
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 一定含有C、H、O三种元素 | |
| B. | 只含有C、H两种元素 | |
| C. | 一定含有C、H两种元素,可能含有O元素 | |
| D. | 无法确定 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 规格 | 250g/袋 |
| 配料 | 氯化钠碳酸钾 |
| 含碘量 | (20-30mg)/lKg |
| 保质期 | 18个月 |
| 食用方法 | 勿长时同炖炒 |
| 贮藏方法 | 避先,避热、密封、防潮 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 表示分子个数 | ① | 表示离子所带电荷数 | ② |
| 表示元素化合价 | ④ | 表示分子中原子的个数 | ③ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
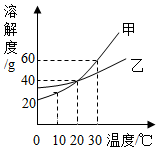 如图所示甲、乙两种固体物体的溶解度曲线.下列说法不正确的是( )
如图所示甲、乙两种固体物体的溶解度曲线.下列说法不正确的是( )| A. | 20℃时,甲的溶解度大于乙 | |
| B. | 10℃时,甲和乙的饱和溶液的溶质质量分数相等 | |
| C. | 30℃时,甲的饱和溶液降至0℃,析出了晶体40g,则原甲的饱和溶液质量为160g | |
| D. | 30℃时,甲和乙的饱和溶液降温至10℃,甲析出的晶体一定比乙多 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com