
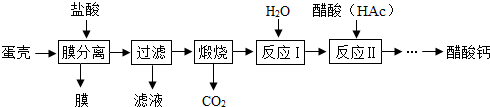
分析 (1)碳酸钙在高温条件下分解生成氧化钙和二氧化碳;
二氧化碳是一种主要的温室气体;
根据反应的化学方程式可以判断反应物之间的质量比;
(2)氢氧化钙的溶解度很小;
(3)氢氧化钙和醋酸反应生成醋酸钙和水;
(4)碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳.
解答 解:(1)煅烧碳酸钙时的化学方程式为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;
CO2的任意排放会引发的环境问题是温室效应;
CO2与CH4一定条件下化合可生成甲醛(HCHO),反应的化学方程式为:CO2+CH4═$\frac{\underline{\;一定条件\;}}{\;}$2HCHO,
则此反应中CO2与CH4的最佳质量比为:44:16=11:4;
a.焚烧秸杆时能够产生大量的二氧化碳;
b.发展火力发电时需要燃烧大量的煤,煤燃烧时能够产生大量的二氧化碳;
c.发展太阳能不会产生二氧化碳.
故填:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;温室效应;11:4;c.
(2)在反应Ⅰ中制备石灰乳,而不是制备澄清石灰水的目的是石灰乳中氢氧化钙的含量高;
熟石灰的水溶液显碱性,可以用来改良酸性土壤.
故填:石灰乳中氢氧化钙的含量高;改良酸性土壤.
(3)在反应Ⅱ中醋酸过量的目的是使氢氧化钙完全反应;
反应Ⅱ的化学方程式为:Ca(OH)2+2HAc═Ca(Ac)2+2H2O.
故填:使氢氧化钙完全反应;Ca(OH)2+2HAc═Ca(Ac)2+2H2O.
(4)膜分离时,盐酸不能过量的主要原因是防止盐酸和碳酸钙反应.
故填:防止盐酸和碳酸钙反应.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
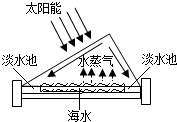 水是生命之源,“爱惜水、保护水”是每个公民的义务和责任.
水是生命之源,“爱惜水、保护水”是每个公民的义务和责任.| 试剂 现象 污水 | 石蕊试液 | 氯化钡溶液 |
| 甲车间 | 变蓝色 | 产生白色沉淀 |
| 乙车间 | 变红色 | 无明显现象 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 为测定某氨肥中硫酸铵的纯度(即质量分数)是否与如图标签相符,小林取一定量该氨肥样品与烧杯中配成溶液与足量氯化钡溶液反应,记录有关数据如下表
为测定某氨肥中硫酸铵的纯度(即质量分数)是否与如图标签相符,小林取一定量该氨肥样品与烧杯中配成溶液与足量氯化钡溶液反应,记录有关数据如下表| 反应前 | 反应后 | |
| 烧杯和样品溶液总质量 | 氯化钡溶液质量 | 过滤后烧杯和溶液总质量(滤液的损失忽略不计) |
| 45g | 55g | 76.7g |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | $\stackrel{-3}{N}$H3--NH3中氮元素显-3价 | B. | 4H--4个氢元素 | ||
| C. | 镁离子--Mg+2 | D. | 氧化亚铁--Fe3O4 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com