
【题目】下列有关说法中,正确的是
①将空气依次通过足量的NaOH溶液、浓硫酸、灼热的铜网,可得到含少量稀有气体的氮气;
②露置在空气中的浓硫酸和浓盐酸,一段时间后溶质质量分数减小的原理相同;
③降低可燃物的着火点是灭火的途径之一;
④Al可以实现单质![]() 氧化物
氧化物![]() 碱的转化;
碱的转化;
⑤实现CuO→Cu的转化,可以利用C、CO、H2的还原性
A. ①⑤B. ①②③C. ②③④D. ①③⑤
【答案】A
【解析】
①将空气依次通过足量的NaOH溶液可除去空气中的二氧化碳,通过浓硫酸可除去空气中的水分,通过灼热的铜网可除去空气中的氧气,最后可得到含少量稀有气体的氮气,说法正确;
②露置在空气中的浓硫酸和浓盐酸,一段时间后浓硫酸因吸水溶剂增加而溶质质量分数减小,浓盐酸因氯化氢气体挥发而溶质减少最后溶质质量分数减小,两者的溶质质量分数减小的原理不相同,原说法错误;
③灭火的原理是破坏燃烧的条件,只要破坏燃烧的任一个条件都可以达到灭火的目的,而着火点是物质的本身属性无法降低,所以原说法错误;
④Al与氧气反应可生成氧化铝,氧化铝不能与水反应,所以不可以实现单质![]() 氧化物
氧化物![]() 碱的转化,原说法错误;
碱的转化,原说法错误;
⑤因为C、CO、H2都可以与氧化铜发生反应生成铜,都是利用C、CO、H2的还原性,说法正确。
故选A。


科目:初中化学 来源: 题型:
【题目】推理是化学学习的一种方法,以下推理正确的是( )
A. 点燃H2与O2混合气体可能爆炸,则点燃CH4与O2的混合气体也可能爆炸
B. 碱性溶液能与二氧化碳气体反应,则能与二氧化碳气体反应的液体pH一定大于7
C. 酸与碱发生中和反应生成盐和水,所以生成盐和水的反应一定是中和反应
D. 稀有气体元素的原子最外层电子数为8(氦除外),因此微粒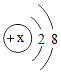 一定是稀有气体元素的原子
一定是稀有气体元素的原子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示,向试管里的水中加入某物质后,U型管中原来相平的红墨水出现如图所示的情况,则加入的物质可能是( )
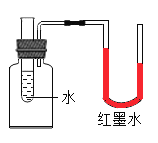
A. 氢氧化钠B. 生石灰C. 浓硫酸D. 硝酸铵
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上炼铁、炼钢和轧制钢材的主要流程如图:
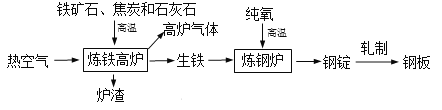
(1)炉渣中含有硅酸钙(CaSiO3),其中硅元素的化合价是___,在高炉中加入石灰石的目的是除去脉石(SiO2)生成炉渣CaSiO3,除去脉石的反应化学方程式是_________。
(2)反应:①Fe2O3 + 3C![]() 2Fe + 3CO↑,②Fe2O3 + 3CO
2Fe + 3CO↑,②Fe2O3 + 3CO![]() 2Fe + 3CO2,用于高炉炼铁的原理是________,属于置换反应的是_________(填序号)。
2Fe + 3CO2,用于高炉炼铁的原理是________,属于置换反应的是_________(填序号)。
(3)炼铁时将铁矿石粉碎的目的__________。
(4)炼钢就是将生铁“降碳除杂(硫、磷等)”,写出炼钢炉中降碳的反应化学方程式_________。
(5)轧制过程是___________变化(填“物理”或“化学”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】北京大学生命科学学院蒋争凡教授研究组发现,锰离子是细胞内天然免疫激活剂和警报素。在元素周期表中锰元素的某些信息如图所示,下列有关锰的说法正确的是_____。
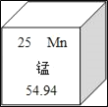
A.原子核内质子数为25
B.属于非金属元素
C.原子核内中子数为25
D._____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组的同学学习“灭火器原理”后,设计了如下图所示实验,并对反应后瓶中残留废液进行探究。
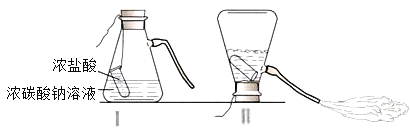
(提出问题)废液中所含溶质是什么?
(猜想与假设)
猜想1:废液中的溶质是NaCl、Na2CO3和HCl
猜想2:废液中的溶质只有NaCl
猜想3:皮液中的溶质是NaCl、HCl
猜想4:废液中的溶质是_____。
(讨论与交流)
小明认为猜想I无需验证就知道是错误的,用化学方程式说明他的理由_____
(实验与结论)
小亮同学为验证猜想3,取少量废液装入试管中,然后滴入酚酞溶液,发现溶液不变色,于是小亮认为猜想3正确。你认为他的结论正确或错误的理由是_____。
请你另设计实验方案验证猜想3:
实验步骤 | 实验现象 | 实验结论 |
_____ | _____ | 猜想3正确 |
(拓展与应用)若废液中的溶质是NaCl和HCl,根据盐酸的性质,无需另加试剂,只要对废液进行_____操作,即可从废液中得到NaCl固体。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示是甲、乙二种物质的溶解度曲线。
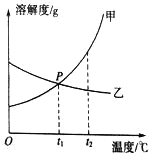
(1)P点的含义是_____。
(2)等质量的甲、乙二种物质的饱和溶液从t2℃降温到t1℃时,甲溶液的质量_____乙溶液的质量(填“>”“<”“=”)。
(3)盐碱湖地区有一种说法:“冬天捞碱,夏天晒盐”,其中“碱”的溶解度曲线与图中_____物质的溶解度曲线相似(填“甲”“乙”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A~I是初中化学常见物质。A与B在高温条件下反应生成C和D,该反应在工业上可用于冶炼金属,A和C是组成元素相同的两种气体,D在气体E中燃烧生成黑色固体B.D与F的溶液反应生成G和H,F可用于配制波尔多液。
(1)固态C的俗名是_____,实验室区分气体A和C的液体试剂为_____。
(2)E、F的化学式分别为_____、_____。
(3)A+B![]() C+D的化学方程式为_____,D+F→G+H的反应类型是_____。
C+D的化学方程式为_____,D+F→G+H的反应类型是_____。
(4)向F的溶液中加入一定量的D,充分反应后,过滤,向滤渣中滴加I的稀溶液,有气泡产生,同时生成G,则滤渣的成分是_____,I的化学式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某校化学兴趣小组的同学在探究金属的化学性质时,发现铜与稀硫酸在常温或加热的条件下均不反应.那么,铜与浓硫酸能否发生反应呢?他们设计了如下图所示装置进行探究.
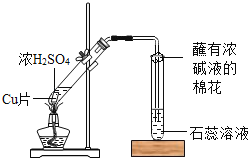
[猜想与假设]
①在常温下能反应
②常温下不能反应,但在加热条件下能反应
③在加热条件下不能反应
[查阅资料]
含有Cu2+的水溶液通常显蓝色
[实验与事实]
操作①将一小块铜片放入试管中,加入足量浓硫酸,无明显现象;
操作②加热该试管,铜片上有气泡,产生了有刺激性气味的气体;
操作③停止加热,将试管中的残液慢慢倒入水中,溶液呈蓝色.
[分析与思考]
(1)甲同学认为,由以上探究可知:猜想_____(填序号)是正确的.
(2)乙同学认为,经检验产生的气体是SO2,所以铜跟浓硫酸在加热条件下反应的产物只是SO2和CuSO4.
(3)丙同学认为,在实验装置中,“蘸有浓碱液棉花”的作用是_____.
[反思与评价]
(4)操作③中,从安全角度考虑_____(填“可以”或“不可以”)将水倒入残液中,其理由是_____.
(5)在[分析与思考](2)中对产物只是SO2和CuSO4的判断是否准确_____(填“是”或“否”),其理由是_____.
[拓展与应用]
(6)根据以上探究和已掌握的知识,该兴趣小组的同学设计了两个用铜制取硫酸铜的实验方案:
①Cu![]() CuSO4; ②Cu
CuSO4; ②Cu![]() CuO
CuO![]() CuSO4
CuSO4
经过对两种方案的讨论、对比,同学们认为方案②具有的优点有_____(填序号),所以工业上制备硫酸铜不是直接利用浓硫酸与铜反应.
A提高铜的利用率 B提高硫酸的利用率
C不产生污染大气的SO2 D不用浓硫酸,安全性好
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com