
【题目】小红和她的同学学习了金属活动性及稀硫酸的一些性质后,对铜与浓硫酸能否发生反应产生了兴趣,并进行了如下探究:
在一支试管中加入一小片铜,再加入少量的浓硫酸,试管中无现象;再给上述试管加热,试管中产生一种有刺激性气味的气体,将反应后的溶液小心地注入到盛有少量水的烧杯中,溶液呈现出明显的蓝色。
(实验分析)
(1)溶液呈蓝色,说明生成了_____(填“物质名称”或“化学式”)。
(2)根据_____,说明产生的气体不可能是氢气,很可能是一种含硫元素的气体。
(查阅资料)
①常见的含硫元素的气体有二氧化硫和硫化氢。
②二氧化硫能使品红溶液褪色,硫化氢不能使品红溶液褪色
(实验探究)将产生的气体_____中,现象为_____。
(实验结论)
在加热条件下,铜能与浓硫酸反应产生二氧化硫气体,写出铜与浓硫酸反应的化学方程式_____。
(拓展延伸)
有元素化合价升降的反应是氧化还原反应,所含元素化合价降低的反应物是氧化剂,所含元素化合价升高的反应物是还原剂,则下列反应中属于氧化还原反应的是_____,H2SO4作氧化剂的是_____。
①Zn+H2SO4(稀)═ZnSO4+H2↑
②C+2H2SO4(浓)![]() CO2+2SO2↑+2H2O↑
CO2+2SO2↑+2H2O↑
③2Cu+O2+2H2SO4![]() 2CuSO4+2H2O
2CuSO4+2H2O
④FeO+H2SO4═FeSO4+H2O。
【答案】CuSO4(或硫酸铜) 已知“有刺激性气味的气体” 通入品红溶液中 品红溶液褪色 Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O ①② ①②
CuSO4+SO2↑+2H2O ①② ①②
【解析】
{实验分析}(1)溶液变蓝,说明有硫酸铜生成,故填CuSO4(或硫酸铜)。
(2)根据已知“有刺激性气味的气体”,因为氢气无味,故说明产生的气体不可能是氢气,很可能是一种含硫元素的气体,故填已知“有刺激性气味的气体”。
{实验探究}检验生成的气体的种类,将产生的气体通入通品红溶液中,品红溶液褪色,证明气体为二氧化硫,故填通入品红溶液中,品红溶液褪色。
{实验结论}
铜能与浓硫酸在加热时反应生成硫酸铜、二氧化硫和水,故反应的化学方程式写为:Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O。
CuSO4+SO2↑+2H2O。
{拓展延伸}
①Zn+H2SO4(稀)═ZnSO4+H2↑中锌的化合价由0价变为+2价,而氢元素的化合价由+1价变为0价,所以属于氧化还原反应,其中硫酸是氧化剂;
②C+2H2SO4(浓)![]() CO2+2SO2↑+2H2O↑碳的化合价由0价变为+4价,而硫元素的化合价由+6价变为+4价,所以属于氧化还原反应,其中硫酸是氧化剂;
CO2+2SO2↑+2H2O↑碳的化合价由0价变为+4价,而硫元素的化合价由+6价变为+4价,所以属于氧化还原反应,其中硫酸是氧化剂;
③2Cu+O2+2H2SO4![]() 2CuSO4+2H2O中没有元素化合价升降的反应,不属于氧化反应反应;
2CuSO4+2H2O中没有元素化合价升降的反应,不属于氧化反应反应;
④FeO+H2SO4=FeSO4+H2O中没有元素化合价的升降,不属于氧化反应反应,属于氧化还原反应的是①②,故填①②;
上述反应中,H2SO4作氧化剂的是①②,故填①②。


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】下列有关计算结果错误的是( )
A. K2Cr2O7中Cr元素的化合价为+6价
B. NH4NO3中氮元素的质量分数为35%
C. C2H4与C4H8中碳元素和氢元素的质量比相同,均为6:2
D. 已知20℃时,NaCl的溶解度为36g,据此计算出该温度下其饱和溶液的质量分数约为26.5%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】青少年看书、写字一定要爱护眼睛,台灯是在光线不足时常用的照明用具。
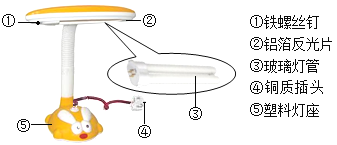
(1)图中序号标示的材料一共分为___________类;
(2)灯管后面的反光片为铝箔。铝块能制成铝箔是利用了铝的___________性;
(3)铝比铁活泼,但铝箔比铁螺丝钉耐腐蚀。铝制品耐腐蚀的原因是(用方程式表示)___________;
(4)为验证铁、铜、铝的活动性顺序,甲乙两位同学设计了不同实验方案,都达到了实验目的。所用的试剂有铝片、铁片、硫酸铝溶液,硫酸亚铁溶液,硫酸铜溶液。实验方案如下:
实验方案 | 方案一 | 方案二 |
实验操作 | 一种金属放入两种溶液中
| 两种金属同时放入一种溶液中
|
①方案一中有关反应的化学方程式是___________;
②方案二中选择的溶液 是___________(写化学式)溶液;
③军军同学又设计了一个新的方案,也能达到实验目的。将三种金属分别放入一种溶液中,该溶液中的溶质在物质分类上和前两位同学所用的试剂不同,他选择的溶液是___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)下面是部分元素原子或离子的结构示意图。请你仔细观察、分析,然后回答问题:

上述粒子中,属于同一种元素的是_____(填序号,下同),属于阳离子的是_____电子层数相同,最外层电子数也相同的粒子有_____
(2)如图是表示某气体分子的示意图,图中“●”和“O”分别表示两种不同质子数的原子,其中表示化合物的是_____

(3)标出氧化镁中镁元素的化合价_____氧化镁中镁元素与氧元素的质量比_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】天然水净化为自来水的主要流程如图1所示:
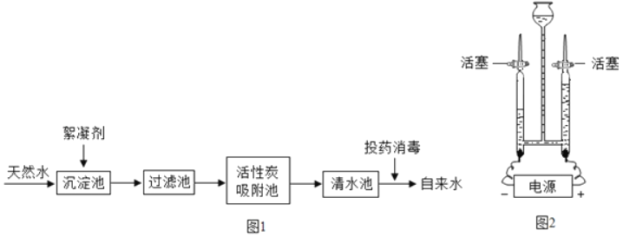
(1)下列说法正确的是_____(填字母)
A.过滤池可以除去难溶性杂质
B.活性炭吸附池可以除去水中的色素和臭味
C.清水池中一定是软水
D.投药消毒发生的是化学变化
(2)明矾(KA1(SO4)m12H2O)能作絮凝剂,是因为明矾溶于水后生成具有吸附作用的胶状物氢氧化铝,m=_____
(3)目前不少自来水用液氯(Cl2)作为消毒剂,液氯注入水后发生反应的示图

其中“![]() ”、“O”“●”代表不同原子,产物D为次氯酸(HClO),有杀菌消毒作用。写出液氯与水反应的化学方程式是_____。
”、“O”“●”代表不同原子,产物D为次氯酸(HClO),有杀菌消毒作用。写出液氯与水反应的化学方程式是_____。
(4)图2是电解水的实验室装置图,写出该反应的化学方程式_____,实验室用“电解水”或氢气在氧气中燃烧的实验探究水的组成元素,理论依据是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲烷制甲醇具有很高的经济价值与社会意义,科学家发现甲烷和水在一定条件下转化为甲醇(CH3OH)同时生成氢气,该反应的化学方程式为_____。将甲醇与氧气混合气体7.2g置于一密闭容器内,在一定条件下完全反应,恢复至室温下测得气体质量减少3.6g,混合气体通过足量澄清石灰水,溶液质量增重2.2g,请写出甲醇与氧气发生反应的化学方程式:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图象分别与选项中的操作相对应,其中合理的是

A. 向一定量稀氢氧化钠溶液中滴入水
B. 向一定量氯化铜溶液中加入一定量铝
C. 向一定量二氧化锰固体中加入一定量过氧化氢溶液
D. 向一定量硫酸和硫酸铜混合溶液中滴入氢氧化钠溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了探究化学反应前后物质的总质量是否发生改变,甲同学和乙同学分别设计了下面两个实验,请回答相关问题:
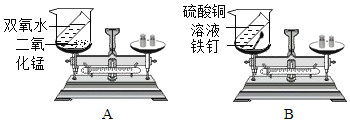
(1)甲同学设计的实验如图A所示,反应前,托盘天平的指针指向刻度盘的中间两种物质反应后,托盘天平___________(填“向左”“向右”或“不”)偏转,原因是____________________________________________。
(2)乙同学设计的实验如图B所示,通过实验得出结论:化学反应前后物质的总质量____________________________________________。
(3)两位同学通过交流反思得到启示:在探究化学反应前后物质的总质量是否发生改变时,对于有气体参加或有气体生成的反应一定要在___________装置中进行。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】蛋白质是由丙氨酸(C3H7NO2)等多种氨基酸构成的。根据内氨酸的化学式计算:
(1)氨基酸由_____种元素组成(写数值);
(2)一个丙氨酸分子中含有_____个原子;
(3)丙氨酸的相对分子质量为_____;
(4)丙氨酸中氮、氢元素的质量比为_____(写最简比)。
(5)178g丙氨酸中含氢元素的质量为_____g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com