
| 实验 序号 | 过氧化氢溶 液浓度/% | 过氧化氢溶 液体积/ml | 温度/ ℃ | 二氧化锰的 量/g | 收集氧气体 积/ml | 反应所需时 间/s |
| Ⅰ | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
| Ⅱ | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
| Ⅲ | 30 | 5 | 35 | 2 | 49.2l | |
| Ⅳ | 30 | 5 | 55 | 2 | 10.76 |
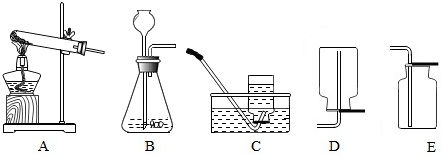
分析 (1)根据药品的状态和反应所需的条件选择发生装置;
(2)过氧化氢分解产生氧气和水,可以据此写出该反应的化学方程式;比较表格中的数据在其他条件都相同时,可以看出过氧化氢的浓度、温度等对化学反应速率的影响;
(3)根据氯酸钾分解生成氧气的化学方程式可知,只有氧气是气体,则可利用反应前后固体的质量差来计算氧气的质量,然后将氧气的质量代入化学方程式来计算生成的氯化钾的质量来解答.
解答 解:(1)制氧气可以用双氧水和二氧化锰,制二氧化碳可以用碳酸钙和稀盐酸,制氢气可以用稀硫酸和锌粒,都是固体和液体反应,条件不需要加热,所以发生装置可用B;故填:B;
(2)从表中分析可知:①②中除了过氧化氢浓度不同之外,其他的各种量均相同,所以可以判断出是反应物的浓度影响了反应速率,并且是浓度越大,反应速率越快;③④则是温度不同其他条件相同,温度高的反应速率快;
故填:反应物浓度; 温度越高,化学反应速率越快;
(3)①因反应中氧气为气体,则氧气质量为30g-25.2g=4.8g;
②二氧化锰的质量为:25.2g×25%=6.3g;
③解:设剩余固体中氯化钾的质量为M,则
2KClO3$\frac{\underline{MnO_2}}{△}$ 2KCl+3O2↑
149 96
M 4.8g
$\frac{149}{M}$=$\frac{96}{4.8g}$
M=7.45g
答:剩余固体中的氯化钾的质量为7.45g;
故答案为:①4.8g;②6.3g;③7.45g.
点评 本题主要考查了能够影响化学反应的因素及利用化学反应方程式的计算,解答这类题时要注意尽可能的把题中的能够影响化学反应的因素找出,然后再利用控制变量法来进行判断,最后得出答案及利用固体质量差分析氧气的质量,然后代入方程式计算即可.


科目:初中化学 来源: 题型:选择题
| A. | 红磷燃烧产生大量的白烟 | |
| B. | 木炭在空气中燃烧,生成二氧化碳气体 | |
| C. | 硫在空气中燃烧,产生淡蓝色火焰 | |
| D. | 铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
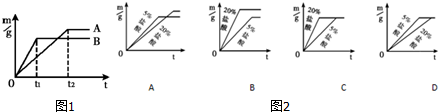
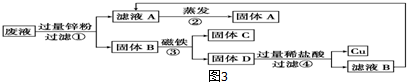
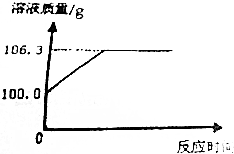 将10.0g铜锌合金的粉末置于烧杯中,然后向其中加入100.0g的稀硫酸溶液,恰好完全反应,测得烧杯中溶液质量的变化关系如下图所示(不考虑物质耗损).
将10.0g铜锌合金的粉末置于烧杯中,然后向其中加入100.0g的稀硫酸溶液,恰好完全反应,测得烧杯中溶液质量的变化关系如下图所示(不考虑物质耗损).查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
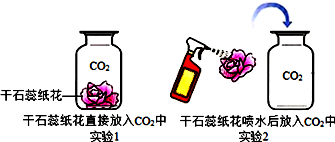
| A. | 气体通入紫色石蕊溶液,溶液颜色变红 | |
| B. | 气体使燃着的木条熄灭 | |
| C. | 在盛满气体的容器中,放入小虫,小虫死去 | |
| D. | 气体通入澄清的石灰水,石灰水变浑浊 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
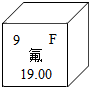 化学是一门富有创造性的科学.含氟物质的合成,对推动社会进步发挥着巨大作用.
化学是一门富有创造性的科学.含氟物质的合成,对推动社会进步发挥着巨大作用.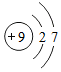 ,由氟原子的结构示意图知,氟原子在化学反应中易得(填“失”或“得”)电子.
,由氟原子的结构示意图知,氟原子在化学反应中易得(填“失”或“得”)电子.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com