
| 实验步骤 | 实验现象 | 实验结论及分析 |
| ①取少量滤液于试管中,滴加足量的NaOH浓溶液后加热,并将湿润的红色石蕊试纸放在试管口。 | | 滤液中含有NH4Cl,有关化学方程式: NaOH + NH4Cl =" NaCl" + NH3↑+ H2O |
| ②另取少量滤液于试管中,滴加稀盐酸。 | 产生无色 无味气体。 | 滤液中含有 ,有关化学方程式: 。 |
| ③另取少量滤液蒸干后充分灼烧,取灼烧后的残余固体溶于水,滴加稀HNO3,再滴加AgNO3溶液。 | 产生白色沉淀。 | 滤液中含有 ,滤液蒸干后充分灼烧的目的是 。 |
| 实验操作 | 实验现象 | 实验结论 |
| 取一定量纯碱样品配成溶液后,滴加过量的CaCl2溶液。 | 产生白色沉淀。 | 反应的化学方程式: 。 |


 53随堂测系列答案
53随堂测系列答案科目:初中化学 来源:不详 题型:单选题
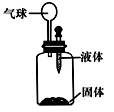
| A.①③ | B.②③ | C.②④ | D.③④ |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
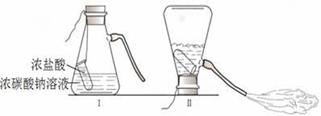
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.长期使用硫酸铵会使土壤呈酸性,应将硫酸铵与熟石灰混合使用 |
| B.生活污水、农药和难分解的有机物等会造成水体污染 |
| C.“酸可以除锈”、“碱可以去油”都是发生了化学变化 |
| D.许多合金比组成合金的纯金属强度和硬度更高、抗腐蚀性能更好 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.NH4+、H+、NO3- | B.H+、Na+、HCO3- |
| C.Fe2+、OH-、SO42- | D.K+、H+、MnO4- |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.K2SO4、KNO3、H2SO4、KMnO4 | B.(NH4)2SO4、HCl、NNO3、K2SO4 |
| C.K2SO4、NaCl、NNO3、Na2CO3 | D.BaCl2、NNO3、KCl、H2SO4 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:推断题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com