
| A. | 公民应增强环保意识,采取低碳、节俭的生活方式,自觉履行环境保护的义务 | |
| B. | 将秸秆综合利用率达100%,以杜绝秸秆焚烧现象 | |
| C. | 增加以燃煤为主的火力发电厂,为城市提供更多的电力保障 | |
| D. | 对工业污水作处理使之符合排放标准,防止水体污染 |
科目:初中化学 来源: 题型:选择题
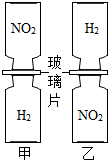 把分别充满红棕色气体NO2和H2的集气瓶,按图甲、乙两种方式放置,然后把两瓶中间的玻璃片都抽走,使两瓶口密合在一起,可观察到图甲中两瓶气体的颜色很快趋于一致(两气体不反应),而图乙中需较长时间才能达到同样的效果.不能由此现象得出的结论是( )
把分别充满红棕色气体NO2和H2的集气瓶,按图甲、乙两种方式放置,然后把两瓶中间的玻璃片都抽走,使两瓶口密合在一起,可观察到图甲中两瓶气体的颜色很快趋于一致(两气体不反应),而图乙中需较长时间才能达到同样的效果.不能由此现象得出的结论是( )| A. | 分子总是不断运动的 | |
| B. | 甲乙现象的差异与气体的密度有关 | |
| C. | 常温常压下,NO2的密度大于H2的密度 | |
| D. | 分子本身都是有大小的 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 南京第二届夏季青奥会上,中国代表团获得金银铜奖牌共计63枚.
南京第二届夏季青奥会上,中国代表团获得金银铜奖牌共计63枚.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
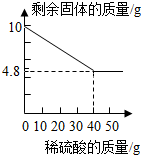
| 实验操作 | 实验现象 | 实验结论 |
| 取少量红色固体加入到足量稀硫酸溶液中 | 若无明显现象 | 假设1成立 |
| 若固体部分(选填“全部”或“部分”)溶解,溶液由无色变蓝色 | 假设2和假设3均成立 |
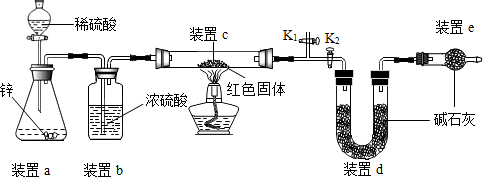
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
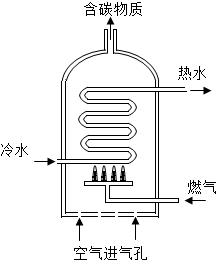 通过化学学习,同学们对物质的组成、结构、性质及用途有了一定的了解.
通过化学学习,同学们对物质的组成、结构、性质及用途有了一定的了解.| 燃料 | 相关燃烧产物的质量/g | |
| CO2 | SO2 | |
| 汽油 | 2900 | 5.0 |
| 天然气 | 2500 | 0.1 |
| 煤 | 2500 | 11.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用灼烧法鉴别羊毛和化纤 | |
| B. | 用肥皂水鉴别硬水和软水 | |
| C. | 加熟石灰粉末研磨,区分氯化铵和硫酸铵 | |
| D. | 用紫甘蓝和酒精溶液制酸碱指示剂 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
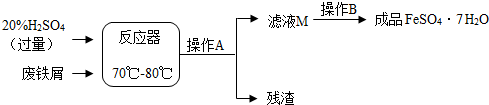
| 温度/℃ | 0 | 10 | 30 | 40 | 50 | 60 | 64 | 70 | 80 | 90 | |
| 溶解度/g | 15.6 | 20.5 | 33.0 | 40.4 | 48.8 | 55.0 | 55.3 | 50.6 | 43.7 | 37.2 | |
| 析出 晶体 | FeSO4•7H2O | FeSO4•4H2O | FeSO4•H2O | ||||||||
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NaC1、K2SO4、Ba(No3)2在水中能大量共存 | |
| B. | 用水可以区分硝酸铵和氢氧化钠两种固体 | |
| C. | 除去稀HCl中少量的H2SO4,可以滴加适量的硝酸钡溶液,然后过滤 | |
| D. | 铜丝在空气中加热后质量会增加,该反应不遵守质量守恒定律 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com