
| A. | N2O5 | B. | N2O3 | C. | N2O | D. | NO2 |
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
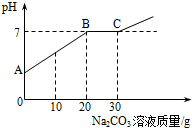 向21.88g含有少量CaCl2的稀盐酸中逐渐滴加10.6%的Na2CO3溶液,加入Na2CO3溶液的质量和溶液pH的关系如图所示.请回答下列问题:
向21.88g含有少量CaCl2的稀盐酸中逐渐滴加10.6%的Na2CO3溶液,加入Na2CO3溶液的质量和溶液pH的关系如图所示.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 煤 | B. | 潮汐能 | C. | 石油 | D. | 天然气 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 序号 | 物质 | 杂质 | 所用试剂和操作方法 |
| A | H2 | HCl | 通过足量的NaOH溶液,干燥 |
| B | NaNO3溶液 | Na2SO4 | 加入过量的Ba(NO3)2溶液,过滤 |
| C | NaCl固体 | Na2CO3 | 加入足量水溶解,过滤 |
| D | 铁粉 | Fe2O3 | 加入适量的稀盐酸,过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com