
分析 (1)根据无机物与有机物的概念来分析;
(2)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析判断.
(3)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
解答 解:(1)由化学式可知,虾青素是一种含碳元素的化合物,属于有机物;故填:有机物;
(2)虾青素的相对分子质量是12×40+1×52+16×4=596,故填:596;
(3)虾青素中碳、氢、氧元素的质量比为(12×40):(1×52):(16×4)=120:13:16;故填:C:H:O=120:13:16.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ① | B. | ② | C. | ③ | D. | ①② |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水是一种最常见的溶剂,自然界中的水中大多数为纯净物 | |
| B. | 水中Ca2+、Mg2+的增多会引起水体的富营养化污染 | |
| C. | 只有用蒸馏的方法才能降低水的硬度 | |
| D. | 在水溶液中发生化学反应,反应速率比较快且充分 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 塑料属于有机合成高分子材料 | |
| B. | 玻璃属于有机高分子合成材料 | |
| C. | 开发使用可降解塑料能有效解决“白色污染”问题 | |
| D. | 合成材料的大量使用给人类带来了严重污染 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
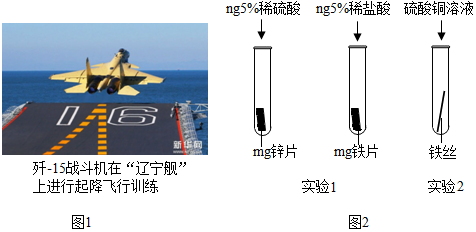
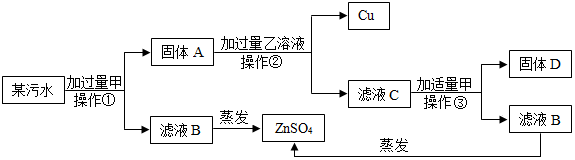
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 一氧化碳 | B. | 二氧化碳 | C. | 水蒸气 | D. | 氮气 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 金属 | 铬 | 铁 | 锌 |
| 反应剧烈程度 | ++ | + | ++++ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com