
| A. | 生石灰 | B. | 硫酸 | C. | 水 | D. | 废铜屑 |
科目:初中化学 来源: 题型:解答题
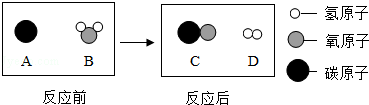
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
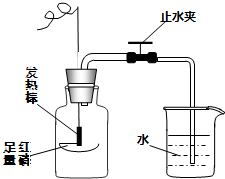 某兴趣小组同学按照下图实验装置进行实验,请回答相关问题:
某兴趣小组同学按照下图实验装置进行实验,请回答相关问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 白酒和白醋--闻气味 | B. | 棉线和羊毛线--灼烧,闻气味 | ||
| C. | 黄铜和黄金--观察颜色 | D. | 食盐和苏打--加醋,观察现象 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 人的胃液里含有适量的盐酸,可以帮助消化,但如果胃酸分泌过多,人会感到胃痛.小军拿来了一种抗酸药(治疗胃酸过多的药物),该药物说明书的部分内容如图所示.
人的胃液里含有适量的盐酸,可以帮助消化,但如果胃酸分泌过多,人会感到胃痛.小军拿来了一种抗酸药(治疗胃酸过多的药物),该药物说明书的部分内容如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验编号 | 实验目的 | 温度 | 催化剂 | 浓度 |
| 甲组实验Ⅰ | 探究浓度对H2O2分解速率的影响 | 25℃ | 二氧化锰 | 10mL 2%H2O2溶液 |
| 甲组实验Ⅱ | 25℃ | 二氧化锰 | 10mL 5%H2O2溶液 |
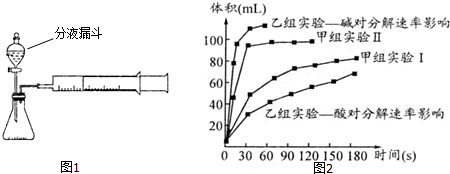
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
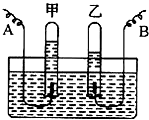 某同学在做电解水实验时,采用了如图所示的简易装置.回答下列问题:
某同学在做电解水实验时,采用了如图所示的简易装置.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com