
【题目】某同学为测定一种石灰石样品中碳酸钙的质量分数,进行如下实验:
①称取25.0g石灰石样品,平均分成两份,并分别加工成块状和粉末状;
②将两份样品分别投入两个锥形瓶中,各加入足量的相同溶质质量分数的稀盐酸(样品所含杂质不溶于水也不与酸反应),测得生成二氧化碳的质量与反应时间的关系如下图所示。请回答:
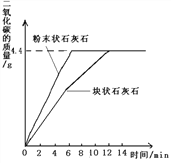
(1)由图中曲线分析得出,影响该化学反应速率的因素是:__________;
(2)每份样品充分反应后.生成二氧化碳的质量为____________.
(3)若每份样品中加入l00.0g稀盐酸,恰好完全反应,求反应后所得溶液中溶质的质量分数为_____________。(要求写出计算过程.不考虑水、氯化氢的逸出.结果精确到0.1%)
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:初中化学 来源: 题型:
【题目】我国著名化学家侯德榜先生,为世界纯碱工业技术的发展做出了杰出贡献。该法以NaCl、NH3、CO2等为原料,先制得NaHCO3,进而生产出纯碱。有关化学反应为:
NH3+CO2+H2O═NH4HCO3
NH4HCO3+NaCl═NaHCO3↓+NH4Cl
2NaHCO3══Na2CO3+CO2↑+H2O
Ⅰ.(1)碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是_____。
a.NaHCO3难溶于水
b.NH4Cl难溶于水
c.NaHCO3的溶解度相对较小,在溶液中首先结晶析出
d.NH4Cl的溶解度相对较小,在溶液中首先结晶析出
(2)某活动小组根据上述原理,模拟碳酸氢钠的制备实验:将二氧化碳气体通入氨化的饱和食盐水中制备碳酸氢钠,实验装置如下图所示。
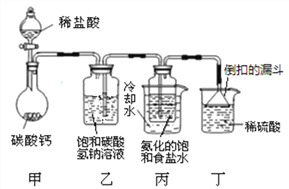
说明:(1)图中夹持、固定用的仪器未画出
(2)“氨化的饱和食盐水”就是向饱和食盐水中通入氨气至饱和
请回答:
①上图装置中有一处不合理,应如何更正_____________;活动小组合理更正装置后,加入试剂进行实验。
②实验结束后,分离出NaHCO3晶体的操作是_____(填操作的名称);
③实验时,为提高二氧化碳的吸收量,须向饱和食盐水中先通入NH3至饱和的原因是______;
Ⅱ.该法所得的纯碱中常含有少量氯化钠,现用下图所示装置来测定纯碱样品中碳酸钠的质量分数(图中夹持、固定用的仪器未画出)。
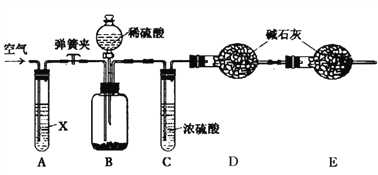
实验步骤如下:
①按上图连接装置,并检查气密性;
②准确称得盛有碱石灰(氢氧化钠和氧化钙的混合物)的干燥管D的质量为83.4g;
③准确称得6.0g纯碱样品放入装置B的广口瓶中;
④打开装置B的分液漏斗旋塞,缓缓滴入稀硫酸,至不再产生气泡为止;
⑤打开弹簧夹,往试管A中缓缓鼓入空气数分钟,然后称得干燥管D的总质量为85.6g。
请回答:
(1)鼓入空气的目的是____________,装置A中试剂X的溶质最适宜选用______(填化学式);
(2)若没有C装置,则会导致测定结果_____(填“偏大”、“偏小”或“不影响”);
(3)根据实验中测得的有关数据,纯碱样品中碳酸钠的质量分数为_____(用百分数表示,结果保留一位小数)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有下列仪器或装置,请回答下列问题:
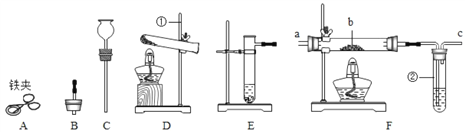
(1)仪器(1)的名称是_____。用废铁屑与稀硫酸反应制取H2,应选择上图仪器中的_____(填字母),该反应的化学方程式为_____;
(2)若用F装置在通风橱内进行CO还原CuO的实验,实验时操作顺序为_____(填序号);
A.先通CO后加热 B.先加热后通CO
(3)用橡皮管、注射器和水,检验 F 装置气密性的操作和现象是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】海洋是个巨大的资源宝库,它不仅孕育着无数的生命,还含有大量的化学物质。
I .从海水中获得氯化钠。将海水进行____________可得到粗盐;为除去粗盐中含有的SO42-、Ca2+、Mg2+等杂质,有如下操作:①溶解;②加过量的Na2CO3溶液; ③加过量的BaCl2溶液;④加适量的盐酸;⑤加过量NaOH溶液;⑥蒸发结晶;⑦过滤。正确的操作顺序是______。(用序号填一种合理组合)。
II.海水提溴。工业上常用“吹出法”制溴,其工艺流程如下:
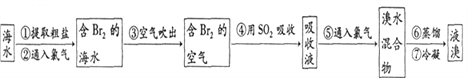
(1)步骤②中的化学方程式为2NaBr+C12=2NaCl+Br2,其反应基本类型_________________。
(2)非金属单质也具有类似金属与盐溶液之间的反应规律,如在溶液中可发生下列反应:C12+2KBr=2KCl+Br2 、Br2+2KI=2KBr+I2
由此可判断C12、I2、Br2活动性由强到弱顺序是 _______________。
III.从海水中得到金属镁。下图是从海水中提取镁的简单流程。
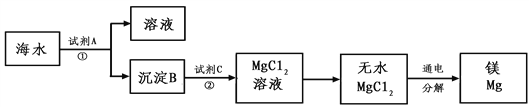
上述过程中,沉淀B与试剂C发生的是中和反应,则沉淀B的化学式为______,由无水MgCl2制取Mg的化学方程式为____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种物质的溶解度曲线如右图所示,据图回答:
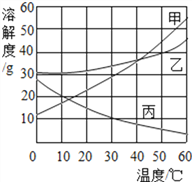
(1)30 ℃时,三种物质的溶解度由大到小的顺序为____________;
(2)要使接近饱和的丙物质溶液变为饱和,可采取的一种措施是________________;
(3)50 ℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至10 ℃时,析出晶体最多的是________,所得溶液中溶质质量分数最大的是_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】归纳总结是学习化学的重要方法,某化学兴趣小组学习碱的性质后,通过实验对氢氧化钙的化学性质进行了验证和总结,如图所示“____”表示物质之间能发生化学反应。请回答问题:

(1)甲同学将酚酞试液滴入氢氧化钙溶液中,观察到溶液变红,得出结论:氢氧化钙溶液呈_____性。乙同学将过量的稀盐酸加入到甲同学所得溶液中,此时所得溶液中含有的溶质有_________
(2)丙同学将碳酸钠溶液加入氢氧化钙溶液中,充分反应后,与乙同学所得溶液混合,静置后发现:上层为无色透明的溶液,底部有白色沉淀,则上层溶液中一定含有的溶质是__________(酸碱指示剂除外),可能含有的溶质是________,为验证可能含有的溶质,可加入试剂_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列A ~ F是初中化学中的六个实验,请按要求填空:
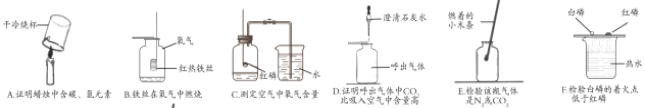
(1)B中反应的化学方程式______________________________,集气瓶中水的作用是_________________。
(2)F装置的实验现象___________________________。
(3)上述实验中不能达到实验目的的是________________(填字母),请选择其中一项说明改进措施_____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】亚硒酸钠(Na2SeO3)可用于提高人体免疫力,硒元素的部分信息如图。下列说法正确的 是
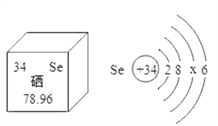
A. 硒元素的原子核外有 78 个电子
B. 硒原子结构示意图中 x=18
C. 1 个硒原子中有 34 个中子
D. 在化学反应中,硒原子容易失去电子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图表示某些物质间转化关系。B、C、D、F、W均为氧化物,C和F组成相同,W和D组成也相同,W有消毒作用;X、Y、G均为单质,E是有机物(部分反应条件或某些反应产物未注明)。回答问题:

(1)化学式:A________、W________。
(2)区分C、F的一种试剂名称为:_______。
(3)物质B在反应③中的作用是_______
(4)反应②的化学方程式:_____________。
(5)工业上可用C和NH3合成尿素【CO(NH2)2】 ,反应中C和NH3的质量比为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com