
分析 (1)根据相对分子质量的计算公式解答;
(2)根据质量分数计算公式解答;
(3)二氧化锰在该反应中作催化剂,反应前后质量不变.
由二氧化锰的质量和剩余固体中二氧化锰的质量分数,可以计算出剩余固体的质量.
(4)根据质量守恒定律知:用原氯酸钾和二氧化锰的质量和去掉剩余固体的质量就是生成氧气的质量.
(5)由生成氧气的质量根据氯酸钾分解的化学方程式可以计算出分解的氯酸钾的质量,由原氯酸钾和分解的氯酸钾的质量可以计算出未分解的氯酸钾的质量.
解答 解:(1)氯酸钾的相对分子质量:39+35.5+16×3=122.5;
(2)氯酸钾中氧元素的质量分数:$\frac{16×3}{122.5}×100%$=39.2%;
(3)剩余固体的质量为:2.0g÷10%=20.0g;
(4)生成氧气的质量为:27.6g+2.0g-20.0g=9.6g;
(5)设未分解的氯酸钾的质量为x.
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
245 96
27.6g-x 9.6g
$\frac{245}{96}=\frac{27.6g-x}{9.6g}$
x=3.1g
答:(1)氯酸钾的相对分子质量为122.5;
(2)氯酸钾中氧元素的质量分数为39.2%;
(3)剩余固体的质量为20.0g;
(4)制得氧气的质量为9.6g;
(5)未分解的氯酸钾的质量为3.1g.
点评 本题主要考查质量守恒定律和有关化学方程式的计算,难度较大.注意:
(1)减少的质量为生成氧气的质量.
(2)剩余固体中含有二氧化锰、未分解的氯酸钾和生成的氯化钾.
(3)原氯酸钾包括未分解的氯酸钾和分解的氯酸钾.


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:初中化学 来源: 题型:选择题
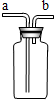
| A. | 氢气从b导管进入可收集氢气 | |
| B. | 瓶内装满水,氢气从b导管进入,可以收集氢气 | |
| C. | 氧气从b导管进入可收集氧气 | |
| D. | 医院给病号输氧,使用该装置用来观测氧气输出的速率,a连节供氧瓶 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
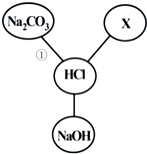 盐酸既是盐化工的重要产品,又是生产硅材料的重要原料.如图归纳出了盐酸与其他物质间相互反应的关系(图中“-”表示相连的两种物质能发生反应).
盐酸既是盐化工的重要产品,又是生产硅材料的重要原料.如图归纳出了盐酸与其他物质间相互反应的关系(图中“-”表示相连的两种物质能发生反应).查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 根据化学式计算:
根据化学式计算:查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 加入7.5gNaOH固体 | B. | 加入12 gNaOH固体 | ||
| C. | 蒸发40g水. | D. | 蒸发30g水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com