
| 实验 | 30% H2O2的质量(g) | 加入的水的体积(mL) | MnO2质量(g) | 收集时间(s) |
| 1 | 10 | 40 | 5 | 200 |
| 2 | 20 | 30 | 5 | 100 |
| 3 | 30 | 20 | 67 |

分析 (1)①根据二氧化锰是固体粉末选择取用装置以及量筒的作用进行分析;
②根据题目中提供的数字结合实验是探究双氧水的溶质质量分数对反应速率的影响分析数据;
③根据数据分析实验结论;
(2)①根据图示可以看出H2O2的用量越多,产生的氧气越多;
②根据图中给出的比例分析;
(3)根据在加热双氧水的过程中一定会有水蒸气散出,使收集的氧气不纯及收集纯净气体的方法分析.
解答 解:(1)①二氧化锰是固体粉末,取用时要用药匙,量取40mL水的实验仪器是量筒和胶头滴管;
②实验探究双氧水的溶质质量分数对反应速率的影响.所以在其他条件相同的情况下进行了三次实验,所以实验3中,加入的二氧化锰质量为5g;
③通过实验中的数据可知,在相同的条件下,双氧水的溶质质量分数越大,反应速率越快,所以相同条件下,实验3产生氧气的速率最快,说明:相同条件下,反应物浓度越大,反应速率越快;
(2)①根据图示可以看出H2O2的用量越多,产生的氧气越多;
②由图示可知3%H2O2溶液8毫升与0.08克MnO2混合,分解速度达到实验要求,若MnO2的质量有4克需要3%H2O2溶液为$\frac{4g}{0.08g}$×8mL=400mL.
(3)在加热双氧水的过程中一定会有水蒸气散出,使收集的氧气不纯,所以将带火星的木条放在导管口没有复燃;为收集到较纯净的氧气,可以采用排水法收集.
故答案为:(1)①药匙;胶头滴管和量筒;②5;③相同条件下,反应物浓度越大,反应速率越快;
(2)①H2O2的用量越多,产生的O2越多;②C;
(3)氧气中混有较多的水蒸气;排水集气.
点评 本题考查实验装置的综合应用,为高频考点,把握反应速率测定原理及影响反应速率的因素为解答的关键,侧重分析与实验能力的考查,题目难度不大.


 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案科目:初中化学 来源: 题型:多选题
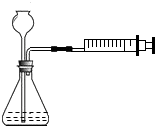
| A. | 推动活塞,若长颈漏斗中液柱不上升,则装置一定漏气 | |
| B. | 推动活塞,若长颈漏斗中液柱不断上升,则装置一定不漏气 | |
| C. | 若装置不漏气,拉动活塞时,长颈漏斗内液面上升 | |
| D. | 若装置不漏气,拉动活塞时,长颈漏斗下端管口产生气泡 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 分子大,原子小 | |
| B. | 分子能保持物质的化学性质,而原子不能 | |
| C. | 分子比原子运动得慢 | |
| D. | 在化学变化中,分子可以再分,而原子不能 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com