
分析 pH=7表示溶液为中性,酸碱两者恰好完全反应.此时加入的氢氧化钠为50g质量分数为16%的,根据这个数值求算硫酸和生成的硫酸钠的质量,进而继续求算硫酸溶液的溶质的质量分数和所得溶液中溶质的质量分数.
解答 解:当pH=7时两者恰好完全反应.
设50g质量分数为16%的氢氧化钠完全反应消耗的硫酸的质量为x,生成的硫酸钠的质量为y.
2NaOH+H2SO4=Na2SO4+2H2O
80 98 142
50g×16% x y
$\frac{80}{50g×16%}$=$\frac{98}{x}$=$\frac{142}{y}$
x=9.8g
y=14.2g
稀硫酸中溶质的质量分数为$\frac{9.8g}{100g}$×100%=9.8%
所得溶液中溶质的质量分数为$\frac{14.2g}{100g+50g}$×100%≈9.5%
答:(1)稀硫酸溶液中溶质的质量分数为9.8%.
(2)当pH=7时所得溶液的溶质质量分数9.5%
点评 根据化学方程式进行计算,首先要确定计算所需要的数据,进而根据正确的化学方程式和相关的相对分子质量计算,注意过程要完整.另外需要求算多个数据时,考虑是否可以通过同一方程式计算,避免计算过程的繁琐.


科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:推断题
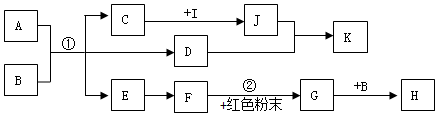
 推断碳和部分碳的化合物间转化关系如图所示
推断碳和部分碳的化合物间转化关系如图所示查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 酿皮子 | B. | 浆水面片 | C. | 拔丝洋芋 | D. | 汪手抓羊肉 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
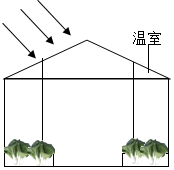 如图所示是一个现代化植物生产车间(温室),植物生长所需的化肥可通过调节二氧化碳来补充.
如图所示是一个现代化植物生产车间(温室),植物生长所需的化肥可通过调节二氧化碳来补充.查看答案和解析>>
科目:初中化学 来源: 题型:推断题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
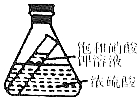 已知浓硫酸(具有强腐蚀性,使用时需注意安全)具有吸水性,可吸收空气中的水蒸气.小明根据这一性质设计了如浓硫酸图所示的趣味实验,一段时间后,小明观察到小试管中有晶体析出.
已知浓硫酸(具有强腐蚀性,使用时需注意安全)具有吸水性,可吸收空气中的水蒸气.小明根据这一性质设计了如浓硫酸图所示的趣味实验,一段时间后,小明观察到小试管中有晶体析出.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 仪器编号 | 所盛试剂的名称 | 试剂或装置的作用 |
| A | 澄清石灰水 | 证明二氧化碳的存在 |
| B | 浓硫酸 | 吸收水煤气中的水蒸气 |
| C | 因为氢气燃烧生成水,看到烧杯内壁上有水珠出现,能证明H2存在 | |
| D | 一氧化碳燃烧生成二氧化碳,二氧化碳能使澄清石灰水变浑浊能证明CO存在 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com