
人类对金属的开发和利用是循序渐进的。
(1)青铜器是人类较早使用的金属制品。西汉时期,人们主要采用“湿法冶金”。如将铁浸入硫酸铜溶液中,该反应的化学方程式为 。
(2)随着技术的不断进步,人们能利用还原剂从金属的氧化物中将其还原出来。例如,
高炉炼铁所涉及的物质转化过程如下:

其中,物质A为 (填化学式),A与赤铁矿中的氧化铁反应的化学方程式为 。
(3)每年因为腐蚀(如铁生锈)而报废的金属相当于年产量的20%~40%,人们采用多
种方法防止金属腐蚀。例如,将清洗后的铁锅擦干后存放可以防止铁锅生锈,其原
因是 。
(4)铝的金属活动性比铁 (填“强”或“弱”),但铝制品却具有比较好的抗腐
蚀性能,其原因是 (用化学方程式说明)。
(1)Fe + CuSO4 = FeSO4 + Cu
(2)CO Fe2O3
+ 3CO  2Fe + 3CO2
2Fe + 3CO2
(3)防止铁与水接触 (其他合理答案均可得分)
(4)强 4Al + 3O2 = 2Al2O3
【解析】
试题分析:(1)依据湿法炼铜的原理可知,铁能与硫酸铜溶液反应,生成铜和硫酸亚铁,故反应的化学方程式为Fe+CuSO4=FeSO4+Cu。
(2)根据题意,二氧化碳在高温的条件下可以与碳反应,生成一氧化碳(化学式为CO),而一氧化碳可与赤铁矿中的氧化铁在高温下反应,生成铁和二氧化碳,故反应的化学方程式为Fe2O3 + 3CO 2Fe + 3CO2。
2Fe + 3CO2。
(3)铁生锈是铁与空气中的水和氧气共同作用的结果,而将清洗后的铁锅擦干,可以防止铁与水接触,从而达到铁锅防锈的目的。
(4)根据金属活动性顺序可知,铝的活动性比铁强,但由于铝能与空气中的氧气反应,生成氧化铝,氧化铝是一种致密的薄膜,附着在铝的表面,从而阻止了铝与氧气的进一步反应,其中反应的化学方程式为4Al+3O2═2Al2O3。
考点:金属的化学性质,铁的冶炼,金属锈蚀的条件及其防护
点评:解答本题,就要熟练掌握金属的性质、冶炼、锈蚀及防护等方面的知识,只有这样才能做出正确解答。


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:初中化学 来源: 题型:
 人类对金属的开发和利用是循序渐进的.
人类对金属的开发和利用是循序渐进的.
| ||
| ||
查看答案和解析>>
科目:初中化学 来源:2013届江苏省泰州市民兴实验中学九年级上学期期末考试化学试卷(带解析) 题型:填空题
人类对金属的开发和利用是循序渐进的。
(1)青铜器是人类较早使用的金属制品。西汉时期,人们主要采用“湿法冶金”。如将铁浸入硫酸铜溶液中,该反应的化学方程式为 。
(2)随着技术的不断进步,人们能利用还原剂从金属的氧化物中将其还原出来。例如,
高炉炼铁所涉及的物质转化过程如下: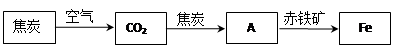
其中,物质A为 (填化学式),A与赤铁矿中的氧化铁反应的化学方程式为 。
(3)每年因为腐蚀(如铁生锈)而报废的金属相当于年产量的20%~40%,人们采用多
种方法防止金属腐蚀。例如,将清洗后的铁锅擦干后存放可以防止铁锅生锈,其原
因是 。
(4)铝的金属活动性比铁 (填“强”或“弱”),但铝制品却具有比较好的抗腐
蚀性能,其原因是 (用化学方程式说明)。
查看答案和解析>>
科目:初中化学 来源:2013-2014学年安徽省安庆市九年级上学期期末化学试卷(解析版) 题型:填空题
人类对金属的开发和利用是循序渐进的.
(1)青铜器是人类较早使用的金属制品.西汉时期,人们主要采用“湿法冶金”.如将铁浸入硫酸铜溶液中,该反应的化学方程式为 _________ .
(2)随着技术的不断进步,人们能利用还原剂从金属的氧化物中将其还原出来.例如,高炉炼铁所涉及的物质转化过程如下:
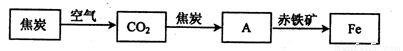
其中,物质A为 _____ (填化学式),A与赤铁矿中的氧化铁反应的化学方程式为 _________ .
(3)每年因为腐蚀(如铁生锈)而报废的金属相当于年产量的20%~40%,人们采用多种方法防止金属腐蚀.例如,将清洗后的铁锅擦干后存放可以防止铁锅生锈,其原因是 _________ .
(4)铝的金属活动性比铁 _________ (填“强”或“弱”),但铝制品却具有比较好的抗腐蚀性能,其原因是 _________ (用必要的文字和化学方程式说明).

查看答案和解析>>
科目:初中化学 来源: 题型:
人类对金属的开发和利用是循序渐进的。
(1)青铜器是人类较早使用的金属制品。西汉时期,人们主要采用“湿法冶金”。如将铁浸入硫酸铜溶液中,该反应的化学方程式为 ▲ 。
(2)随着技术的不断进步,人们能利用还原剂从金属的氧化物中将其还原出来。例如,高炉炼铁所涉及的物质转化过程如下:
其中,物质A为 ▲ (填化学式),A与赤铁矿中的氧化铁反应的化学方程式为 ▲ 。
(3)每年因为腐蚀(如铁生锈)而报废的金属相当于年产量的20%~40%,人们采用多种方法防止金属腐蚀。例如,将清洗后的铁锅擦干后存放可以防止铁锅生锈,其原因是 ▲ 。
(4)铝的金属活动性比铁 ▲ (填“强”或“弱”),但铝制品却具有比较好的抗腐蚀性能,其原因是 ▲ (用必要的文字或化学方程式说明)

查看答案和解析>>
科目:初中化学 来源: 题型:
人类对金属的开发和利用是循序渐进的.
(1)青铜器是人类较早使用的金属制品.西汉时期,人们主要采用“湿法冶金”.如将铁浸入硫酸铜溶液中,该反应的化学方程式为 _________ .
(2)随着技术的不断进步,人们能利用还原剂从金属的氧化物中将其还原出来.例如,高炉炼铁所涉及的物质转化过程如下:
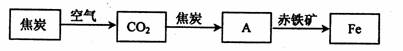
其中,物质A为 _________ (填化学式),A与赤铁矿中的氧化铁反应的化学方程式为 _________ .
(3)每年因为腐蚀(如铁生锈)而报废的金属相当于年产量的20%~40%,人们采用多种方法防止金属腐蚀.例如,将清洗后的铁锅擦干后存放可以防止铁锅生锈,其原因是 _________ .
(4)铝的金属活动性比铁 _________ (填“强”或“弱”),但铝制品却具有比较好的抗腐蚀性能,其原因是 _________ (用必要的文字和化学方程式说明).

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com