
| A. | 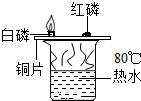 证明可燃物燃烧需要氧气 | B. | 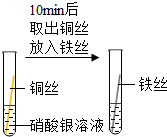 比较Fe、Cu、Ag的金属活动性 | ||
| C. |  常温下配制浓度为2%的石灰水 | D. | 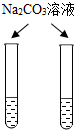 鉴别稀盐酸与稀硫酸 |
分析 可燃物燃烧的条件是:与氧气接触,温度达到可燃物的着火点,二者必须同时具备,缺一不可;
铁比铜活泼,铜比银活泼;
氢氧化钙的溶解度很小;
碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,和稀硫酸反应生成硫酸钠、水和二氧化碳.
解答 解:A、实验过程中,白磷燃烧,红磷不能燃烧,说明白磷的着火点比红磷低,不能说明燃烧需要氧气,该选项不能达到实验目的;
B、向硝酸银溶液中加入铜丝时,铜丝表面附着一层银白色固体,说明铜比银活泼,再加入铁丝时,铁丝表面附着一层黑色固体,说明铁比铜活泼,该选项能够达到实验目的;
C、氢氧化钙微溶于水,2g氢氧化钙不能完全溶解在98g水中,即不能配制2%的氢氧化钙溶液,该选项不能达到实验目的;
D、实验过程中,都产生气泡,无法鉴别稀盐酸和稀硫酸,该选项不能达到实验目的.
故选:B.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:初中化学 来源: 题型:选择题
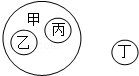 如图表示物质类别相互间存在的关系(其中甲包含乙和丙,不包含丁),下表四个选项中符合如图关系的是( )
如图表示物质类别相互间存在的关系(其中甲包含乙和丙,不包含丁),下表四个选项中符合如图关系的是( )| 甲 | 乙 | 丙 | 丁 | |
| A | 纯净物 | 单质 | 化合物 | 有机物 |
| B | 合成材料 | 合成纤维 | 合成橡胶 | 塑料 |
| C | 盐 | 食盐 | 纯碱 | 火碱 |
| D | 化石燃料 | 石油 | 煤 | 天然气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
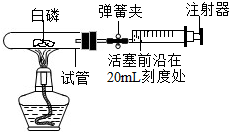 为测定空气中氧气的含量,小华同学打算设计如下方案:选用实际容积为40mL的试管作为反应容器,将过量的白磷放入试管,用橡皮塞塞紧试管,通过导管与实际容积为60mL且润滑性很好的针筒注射器组成如图的实验装置.假设此实验能够按照小华的设想正常进行,且白磷所占体积与导管内的气体体积忽略不计,请回答下列问题:
为测定空气中氧气的含量,小华同学打算设计如下方案:选用实际容积为40mL的试管作为反应容器,将过量的白磷放入试管,用橡皮塞塞紧试管,通过导管与实际容积为60mL且润滑性很好的针筒注射器组成如图的实验装置.假设此实验能够按照小华的设想正常进行,且白磷所占体积与导管内的气体体积忽略不计,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 加入稀盐酸质量/g | 9.6 | 9.8 | 9.9 | 10.0 | 10.1 |
| 溶液的pH | 12.4 | 12.1 | 11.8 | 7.0 | 2.2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向氢氧化钠固体中加入水 | 氢氧化钠固体消失 | 氢氧化钠与水发生了化学反应 |
| B | 用导管分别对准浸没在热水和冷水中的白磷通氧气 | 热水中的白磷燃烧, 冷水中的白磷不燃烧 | 燃烧条件之一是温度达到着火点 |
| C | 向溶质的质量分数为5%的过氧化氢溶液中加入少量氧化铜 | 有大量气泡产生 | 氧化铜起催化作用 |
| D | 向盐酸和氢氧化钙反应后的溶液中滴加酚酞 | 无明显现象 | 说明盐酸和氢氧化钙恰好反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com