

分析 根据A、B、C、D、E为初中化学常见的物质,A为红色金属单质,所以A为铜,铜和氧气加热会生成氧化铜,所以B为氧化铜,B与过量的硫酸反应生成的X溶液为硫酸和硫酸铜溶液,X溶液和C反应生成了浅绿色溶液、铜和无色气体E,所以C为铁单质,亚铁离子在溶液中显浅绿色,所以D为硫酸亚铁,铁和硫酸反应会生成硫酸亚铁和氢气,所以E为氢气,然后结合题中的转化关系进行验证即可.
解答 解:(1)A、B、C、D、E为初中化学常见的物质,A为红色金属单质,所以A为铜,铜和氧气加热会生成氧化铜,所以B为氧化铜,B与过量的硫酸反应生成的X溶液为硫酸和硫酸铜溶液,X溶液和C反应生成了浅绿色溶液、铜和无色气体E,所以C为铁单质,亚铁离子在溶液中显浅绿色,所以D为硫酸亚铁,铁和硫酸反应会生成硫酸亚铁和氢气,所以E为氢气,经过验证,推导正确,所以B是CuO,D是FeSO4;
(2)氧化铜和硫酸在加热的条件下反应生成硫酸铜和水,化学方程式为:CuO+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+H2O;
(3)氧化铜和过量的硫酸反应,所以X溶液中含有的溶质有2种,分别是:H2SO4、CuSO4;
(4)铁和硫酸反应生成硫酸亚铁和氢气,该反应属于置换反应,化学方程式为:Fe+H2SO4=FeSO4+H2↑.
故答案为:(1)CuO,FeSO4;
(2)CuO+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+H2O;
(3)2,H2SO4、CuSO4;
(4)Fe+H2SO4=FeSO4+H2↑,置换.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
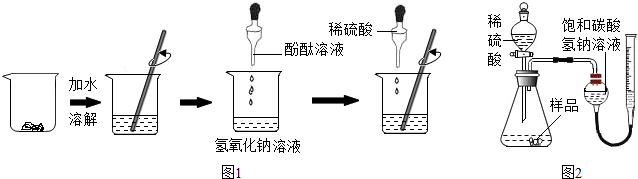
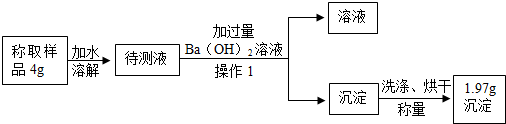
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
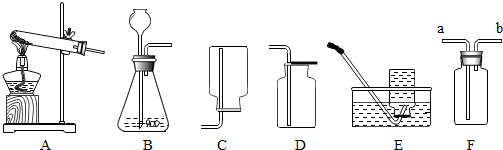
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 滴数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 |
| PH | 13.4 | 13.3 | 13.2 | 13.0 | 12.8 | 12.96 | 12.4 | 4.5 | 1.6 | 1.4 | 1.3 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 稀盐酸用于除铁锈--酸能与金属氧化物反应 | |
| B. | 洗涤剂去除油污--溶解作用 | |
| C. | 区分硬水与软水--加肥皂水搅拌 | |
| D. | 区分羊毛纤维与合成纤维--灼烧后闻气味 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com