
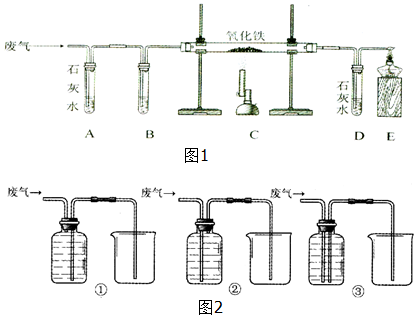
分析 一氧化碳是一种中性气体,不与酸或碱反应,而二氧化碳是一种酸性气体,能与碱反应.所以我们在除去一氧化碳中的二氧化碳气体时,可以选择碱性溶液.
解答 解:(1)为了确定废气的组成,我们利用澄清的石灰水来检验二氧化碳气体,然后再利用氢氧化钠溶液来吸收二氧化碳,然后再利用一氧化碳的还原性,来检验生成的气体是二氧化碳.
(2)一氧化碳具有还原性,所以能使红色固体逐渐变为黑色
(3)A装置用来检验原气体中含有二氧化碳,而D装置用来检验一氧化碳反应的产物二氧化碳.
(4)我们利用洗气瓶来除去二氧化碳并收集一氧化碳气体时,应长管进气.同时需要收集CO,所以还是储气瓶,所以液体还应该是从长管出,所以两个管都应该通到底部.
故答案为:
(1)充分吸收废气中的二氧化碳;
(2)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
(3)A装置用来检验废气中是否含有二氧化碳;D装置用来检验反应中是否有二氧化碳生成,进而推断出废气中是否含有一氧化碳.
(4)③
点评 我们在检验一氧化碳气体时,利用一氧化碳的还原性,然后检验是否有二氧化碳生成,所以我们在检验一氧化碳时,先将二氧化碳气体吸收干净.


科目:初中化学 来源: 题型:选择题
| A、化学之最 | B、化学与生活 |
| ①天然存在的最硬的物质:金刚石 ②地壳中含量最高的金属元素:铁 | ①煤气泄露:开排风扇 ②水壶中的水垢:用食醋除去 |
| C、性质与用途 | D、环境保护 |
| ①木炭有可燃性:作燃料 ②稀有气体通电后发出有色光:作电光源 | ①废旧电池:随意丢弃 ②工业污水:处理后排放 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 化学能帮助我们更好地认识生活、改善生活.西兰花是一种具有防癌抗癌作用的食材,含有蛋白质、维生素C、纤维素和钙、铁、锌、硒等.
化学能帮助我们更好地认识生活、改善生活.西兰花是一种具有防癌抗癌作用的食材,含有蛋白质、维生素C、纤维素和钙、铁、锌、硒等.查看答案和解析>>
科目:初中化学 来源: 题型:推断题
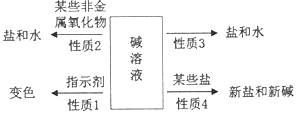 归纳总结是学习化学的一种方法.请结合小明同学对碱的四点化学性质的归纳图完成下列问题.(箭头上方的物质是指与碱反应的物质)
归纳总结是学习化学的一种方法.请结合小明同学对碱的四点化学性质的归纳图完成下列问题.(箭头上方的物质是指与碱反应的物质)查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氢氧化钠 纯碱NaOH 碱 | |
| B. | 氧化钙 生石灰 CaO 氧化物 | |
| C. | 氢氧化钙 消石灰 Ca(OH)2 盐 | |
| D. | 固态二氧化碳 干冰 CO2 有机物 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | C3H5O | B. | C2H8 N2 | C. | C2H8 | D. | C2H5N |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com