
【题目】高纯氧化锌广泛应用于电子工业,某研究小组设计如图流程制备高纯氧化锌:
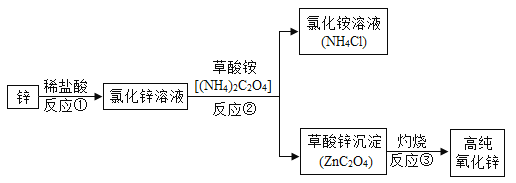
⑴反应②的化学方程式为______________________,所属基本反应类型是_____________。
⑵反应②后进行的分离操作名称是_____________,若得到的氯化铵溶液仍然浑浊,原因可能是_____________(写出一种即可)。
⑶反应③的化学方程式是:ZnC2O4![]() ZnO+CO+X,则X的化学式为_______。
ZnO+CO+X,则X的化学式为_______。
【答案】(NH4)2C2O4+ ZnCl2=ZnC2O4↓+2NH4Cl复分解反应过滤过滤时液面高于滤纸边缘或滤纸破损或仪器不干净CO2
【解析】
(1)由题意可知,氯化锌与草酸铵反应生成了氯化铵和草酸锌沉淀,反应的化学方程式是:ZnCl2+(NH4)2C2O4═ZnC2O4↓+2NH4Cl;是两种化合物相互交换成分生成两种新的化合物,为复分解反应;
(2)反应②后进行的分离,是不溶性物质和溶液的分离,该操作为过滤,完成该操作所需要的玻璃仪器除烧杯、玻璃棒外,还需要漏斗;若得到的氯化铵溶液仍然浑浊,原因可能是过滤时液面高于滤纸边缘或滤纸破损或仪器不干净;
(3)根据反应前后原子的种类、数目不变,可推知x的化学式为CO2。


科目:初中化学 来源: 题型:
【题目】写出下列化学反应的文字表达式(要求写反应现象的写反应现象)。
(1)硫在氧气中燃烧 _____________,反应现象为_______________。
(2)在空气中点燃镁条________,反应现象为_______________。
(3)实验室在常温下制氧气的原理_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种固体物质(均不含结晶水)的溶解度曲线如图所示,下列说法错误的是( )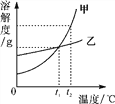
A. t2 ℃时,将甲、乙的两种饱和溶液分别降温到t1 ℃,所得溶液都是饱和溶液
B. t1 ℃时,向50 g水中加入甲可得80 g饱和溶液,则乙在该温度下的溶解度为60 g
C. 甲中混有少量乙时,可用降温结晶的方法提纯甲
D. t2 ℃时,将等质量的甲、乙两种溶液分别降温到0 ℃,甲溶液的溶质质量分数一定小于乙溶液的溶质质量分数
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn粉,溶液质量与加入Zn粉的质量 关系如图所示。下列说法不正确的是

A. a点溶液溶质为AgNO3、Cu(NO3)2和Zn(NO3)2
B. b点溶液为蓝色
C. 取c点的固体滴加稀盐酸,无气泡产生
D. d点溶液中溶质为Zn(NO3)2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】一种有趣的钟表式元素周期表如图所示,关于时针所对应的元素说法中正确的是_____

A.12:00对应的元素为金属元素
B.10:00对应的元素易形成化合物
C.9:00对应元素的离子符号为F+
D.该钟表的整点时间与原子结构中的_________数目相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是氯气和水反应的微观示意图。![]() 表示氯原子,
表示氯原子,![]() 表示氧原子,
表示氧原子,![]() 表示氢原子。
表示氢原子。
![]()
(1)写出图中反应的化学方程式_____________。
(2)已知 HClO 是一种酸,能与 NaOH 反应生成 NaClO,请写出将氯气通入到 NaOH 溶液中发生反应的化学方程式____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是物质与其构成粒子之间的关系图。
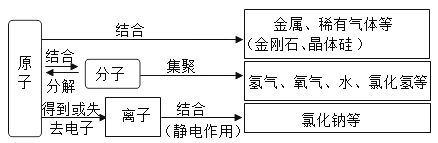
回答下列问题。
(1)金属铁是由________(填“原子”“分子”或“离子”,下同)构成的,硫酸铜是由________构成的。
(2)原子得到或失去电子后形成离子。某离子的结构示意图为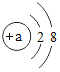 。
。
①当a=________时,该粒子是原子。
②当a=8时,该粒子是________(填“原子”“阳离子”或“阴离子”),其符号为________。
(3)氯化氢是一种无色有刺激性气味的气体,走进实验室就闻到了这种气味。从分子的角度解释这种现象:__________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学要探究燃烧的条件和空气中氧气的含量,进行了如下图所示实验。
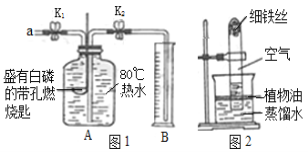
(实验一)(已知:白磷的着火点为40℃)按图1进行实验,实验步骤及现象如下:
步骤Ⅰ.检验装置的气密性,气密性良好。
步骤Ⅱ.将盛有白磷的带孔燃烧匙伸入A瓶中,白磷不燃烧。
步骤Ⅲ.向A瓶中加满80℃热水,塞紧瓶塞,白磷不燃烧。
步骤Ⅳ.打开K1、K2,从a口向瓶中鼓入空气,待瓶中的液面低于燃烧匙底部时,关闭K1、K2。此时进入量筒B中水的体积为200mL,观察到A瓶中的白磷燃烧。
⑴对比步骤Ⅱ和Ⅳ的现象可知,可燃物燃烧的条件之一是____________________。
⑵待装置冷却一段时间后,打开K2,如果观察到__________________,说明空气中氧气的体积约占1/5。若实验测得空气中氧气的体积分数小于1/5,原因可能是_______________(答一条即可)。
(实验二)用图2所示装置,利用铁生锈的原理也可以比较准确地测出空气中氧气的含量。若将此装置中的细铁丝换成足量的细铜丝进行实验,能否比较准确地测出空气中氧气的含量,并说明理由__________________________(已知:铜能与空气中氧气、水、二氧化碳反应生成铜绿。化学方程式:
2Cu+O2+H2O+CO2═Cu(OH)2CO3)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学进行如下图的两个实验。
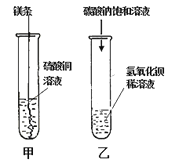
(l)甲实验观察到的现象是________________,溶液由蓝色变成无色。
(2)乙实验中反应的化学方程式为___________;
(3)把甲、乙反应后的溶液倒入同一烧怀,发现有白色沉淀生成。他决定对白色沉淀的成分进行探究。
(查阅资料)硫酸钡不溶于酸。
(提出猜想)白色沉淀为:Ⅰ.________Ⅱ.Mg(OH)和BaSO4;Ⅲ. Mg(OH)2和MgCO3.
(实验方案)
实验操作 | 实验现象与结论 |
过滤、洗涤白色沉淀备用;向白色沉淀中加入盐酸至过量 | ①沉淀全部溶解,且无其它现象;猜想Ⅰ成立;其化 学反应方程式为 ________________________。 ②若_________________且无气体产生,猜想Ⅱ成立。 ③若沉淀完全溶解,_______________,猜想Ⅲ成立。 |
(拓展与思考)如果猜想Ⅲ成立,产生此结果的原因是做乙实验时______________;
上述白色沉淀的成分不可能出现的组合是Mg(OH)2、MgCO3和BaSO4,原因是________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com