
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |
分析 根据已有的知识进行分析,根据表格即可查出硝酸钾在10℃时的溶解度;根据硝酸钾的溶解度确定硝酸钾能否全部溶解,再计算其溶液的质量;要分离硝酸钾和氯化钠的混合物,可以采用降温结晶的方法;根据具体的溶解度判断其温度范围;根据图示结合具体的数据判断溶液的状态,据此解答.
解答 解:
(1)根据表格即可查出40℃时,NaCl的溶解度为36.6g,
(2)称取31.6gKNO3固体时,发现托盘天平指针偏右,说明KNO3偏少,故接下来的操作是继续加KNO3固体至天平平衡;
(3)当KNO3的溶液中含有少量NaCl,由于硝酸钾的溶解度受温度影响大,而氯化钠的溶解度受温度影响不大,所以提纯KNO3所采用的方法为降温结晶(或冷却热饱和溶液),
(4)60℃时,NaCl和KNO3的溶解的分别是37.3g和110g,因此等质量的饱和溶液,KNO3溶液中的溶剂质量较小,将等质量的两物质的饱和溶液分别降温至20℃,都是饱和溶液,由图表格中的数据判知,析出晶体的质量KNO3>NaCl,而溶剂质量不变,则溶液质量:KNO3<NaCl;故选AC.
故答案为:
(1)36.6g;
(2)C;
(3)降温结晶(或冷却热饱和溶液);
(4)A,C.
点评 本题考查了溶解度的有关知识,完成此题,可以依据题干提供的信息结合溶解度的概念进行.


 应用题作业本系列答案
应用题作业本系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
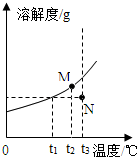 如图为A物质的溶解度曲线.M、N两点分别表示A物质的两种溶液.下列做法不能实现M、N间的相互转化的是(A从溶液中析出时不带结晶水)( )
如图为A物质的溶解度曲线.M、N两点分别表示A物质的两种溶液.下列做法不能实现M、N间的相互转化的是(A从溶液中析出时不带结晶水)( )| A. | 从N→M:先向N中加入适量固体A再降温到t2 | |
| B. | 从N→M:先将N降温到t1再加入适量固体A | |
| C. | 从M→N:先将M降温到t1再将其升温 | |
| D. | 从M→N:先将M升温到t3再加入适量的水 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 2Fe+6HCl═2FeCl3+3H2↑ | B. | NaOH+H2SO4═NaSO4+H2O | ||
| C. | 4Al+3O2═2Al2O3 | D. | CaCO3+Ba(OH)2═BaCO3↓+Ca(OH)2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 除去硫酸镁溶液中混有的少量硫酸和硫酸铜,加入足量镁粉 | |
| B. | 除去CaCl2溶液中的HCl,加入过量的碳酸钙 | |
| C. | 鉴别涤纶和羊毛面料,分别取样灼烧、闻气味 | |
| D. | 除去氯化氢气体中的水蒸气,用氢氧化钠固体 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 冰、干冰、天然气 | B. | 氮气、氧气、空气 | ||
| C. | 水银、水、碘酒 | D. | 石墨、熟石灰、盐酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com