
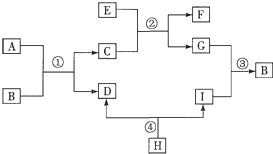
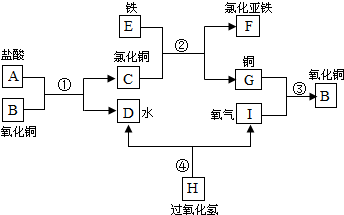
| ||
| ||
| ||


 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案科目:初中化学 来源: 题型:

| 铁的氧化物 | Fe2O3 | Fe3O4 | FeO |
| 颜色 | 红棕 | 黑 | 黑 |
| 物理性质 | 不能被磁铁吸引 | 能被磁铁吸引 | 不能被磁铁吸引 |
| 化学性质 | 可溶于稀硫酸,但不生成气体 | 常温下不溶于稀硫酸 | 可溶于稀硫酸,但不生成气体 |
| 方案 | 实验操作 | 可能的现象 | 结论 |
| ① | 取适量黑色粉末A用磁铁吸引 | 黑色粉末全部被吸引 | 猜想①正确 |
| ② | 取适量黑色粉末A用磁铁吸引 | 黑色粉末部分被吸引 | 猜想②正确 |
| ③ | 猜想③正确 |

| 加入足量的稀H2SO4 |
| 充分反应后 |
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
 某班同学做常见酸和碱与酚酞反应的实验,本次实验后废液分别集中到一个废液缸中.负责清洁实验室的小雪、小丽、小明和小华四位同学围绕如何处理“废液”展开了讨论:
某班同学做常见酸和碱与酚酞反应的实验,本次实验后废液分别集中到一个废液缸中.负责清洁实验室的小雪、小丽、小明和小华四位同学围绕如何处理“废液”展开了讨论:查看答案和解析>>
科目:初中化学 来源: 题型:
 如图所示,物质王国的“小朋友”们手拉手围成一圈做游戏.
如图所示,物质王国的“小朋友”们手拉手围成一圈做游戏.查看答案和解析>>
科目:初中化学 来源: 题型:
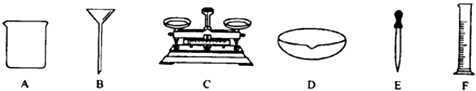
 指出如图中的错误操作
指出如图中的错误操作查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com