
【题目】(1)某物质R完全燃烧的化学方程式为:2R+3O2![]() 2CO2+4H2O,R的相对分子质量等于__。R中碳、氢两种元素质量比等于__。__gR中氢元素质量和18g水氢元素质量相等。
2CO2+4H2O,R的相对分子质量等于__。R中碳、氢两种元素质量比等于__。__gR中氢元素质量和18g水氢元素质量相等。
(2)在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化见下表。下列说法中不正确的是_____。
物质 | 甲 | 乙 | 丙 | 丁 |
反应前物质质量/g | 8 | 32 | 5 | 4 |
反应后物质质量/g | 16 | 4 | x | 24 |
A 该反应为分解反应
B 甲、乙两种物质间参加反应的质量比为1:4
C 丙可能为该反应的催化剂
D 乙、丁两种物质间反应的质量比为7:5
【答案】32 3:1 16 B
【解析】
(1)由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式,反应前碳、氢、氧原子个数分别为0、0、6,反应后的生成物中碳、氢、氧原子个数分别为2、8、8,根据反应前后原子种类、数目不变,2R分子中含有2个碳原子、8个氢原子和2个氧原子构成,则每个R分子由1个碳原子、4个氢原子和1个氧原子构成,则物质X的化学式为CH4O.则R的相对分子质量等于12+1×4+16=32。R中碳、氢两种元素质量比等于(12×1):(1×4)=3:1。需要R的质量为18g×![]() ×100%÷(
×100%÷(![]() ×100%)=16g。
×100%)=16g。
(2)由表中数据分析可知,反应前后甲的质量增加了16g﹣8g=8g,故是生成物,生成的质量为8g;同理可以确定乙是反应物,参加反应的质量为32g﹣4g=28g;丁是生成物,生成的质量为24g﹣4g=20g;由质量守恒定律,丙的质量应不变,可能作该反应的催化剂,也可能没有参加反应。
A、该反应的反应物为乙,生成物是甲和丁,符合“一变多”的形式,属于分解反应,故选项说法正确。
B、甲、乙两种物质间参加反应的质量比为8g:28g=2:7,故选项说法错误。
C、丙的质量应不变,可能作该反应的催化剂,也可能没有参加反应,故选项说法正确。
D、乙、丁两种物质间反应的质量比为28g:20g=7:5,故选项说法正确。
故答案为:
(1)32;3:1;16;
(2)B。


科目:初中化学 来源: 题型:
【题目】(1)镁条具有抗腐蚀性,是因为表面生成了一层氧化物膜,化学实验小组同学为研究镁条表面氧化程度,将3.2g镁条放入一定浓度的稀盐酸中充分反应,测得产生的气体质量与稀盐酸的质量关系如图所示(假设镁条除有MgO外,不含其他杂质)。
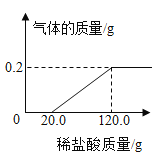
(1)生成氢气的质量为________g。
(2)该镁条中MgO的质量分数为?。
(3)所用稀盐酸中溶质的质量分数为多少?(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C三种物质的溶解度曲线如图所示,请回答下列问题:
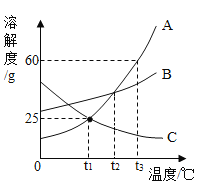
(1)t2℃时,A、B、C三种物质溶解度的大小关系是_____(用“A、B、C”和“>、<、=”表示)
(2)要使接近饱和的C溶液在保持溶质质量分数不变的情况下变成饱和溶液的方法是_____。
(3)将100g质量分数为30%的A溶液由t3℃降温至t1℃,降温后所得溶液中溶质的质量分数是_____。
(4)t3℃时,A、B、C三种物质的混合溶液中,A、B、C三种溶质的质量相等,将混合溶液在该温度下恒温蒸发溶剂,首先析出的物质是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某工业废液中含有CuSO4、ZnSO4、FeSO4,如果将废液直接排放就会造成水污 染。于是几位同学设计实验处理废液,回收工业重要原料硫酸锌和有关金属。实验过程如下:
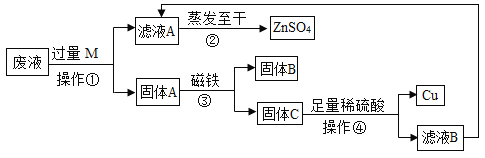
请回答:
(1)操作①的名称是_______,其中玻璃棒的作用是______。写出加过量M发生的一个化学反应的方程式____________________。
(2)固体A中一定有_______。判断操作④中稀硫酸足量的方法是_______。
(3)滤液 A、滤液B合起来蒸发至干目的是_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列化学符号中数字“2”表示的意义不正确的是( )
A.2NH4+:两个铵根离子
B.H2O:一个水分子中含有两个氢分子
C.Zn2+:一个锌离子带两个单位的正电荷
D.![]() :氧化铜中铜元素的化合价为正二价
:氧化铜中铜元素的化合价为正二价
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】20℃时,将 52 g 一定溶质质量分数的甲溶液恒温蒸发水,烧杯中析出固体甲的质量(m 甲)随蒸发水的质量(m 水)变化如下图曲线Ⅰ所示。请回答下列问题:
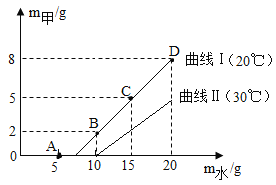
(1)A 点对应的溶液是_______溶液(填“饱和”或“不 饱和”)。
(2)若 30℃ 时恒温蒸发的二者的关系如图中曲线Ⅱ所 示,则甲的溶解度随的升高而_____(填“增大” 或“减小”)。
(3)B 点对应溶液的质量为_____g。
(4)20℃时甲的溶解度为_____g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】兴趣小组设计实验验证草酸亚铁晶体热分解的气体产物,并用热重法(TG)确定其分解后所得固体产物的组成。
资料链接:①草酸亚铁晶体( FeC2O4﹒2H2O)是浅黄色、难溶于水、受热易分解的固体。
②无水硫酸铜遇水会变成蓝色。
探究一: 探究草酸亚铁晶体热分解的气体产物
[猜想假设]猜想一: X、CO2
猜想二: X、CO
猜想三: X、CO、CO2,物质X为________(填化学式)。
[设计实验]
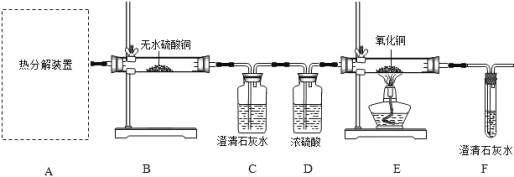
(1)选择_________(填字母序号)作为虚线中的“热分解装置”
A 过氧化氢分解制氧气的发生装置
B 氯酸钾分解制氧气的发生装置
(2)进行上述实验时,先点燃热分解装置中的酒精灯,一段时间后再点燃E处的酒精灯,原因是_________。
(3)D中浓硫酸的作用是________,实验过程中观察到______的现象,证明猜想三正确。
[交流讨论]
(1)C中反应的化学方程式为__________。
(2)该装置并不能严谨证明猜想三成立,改进的措施是在C和D装置之间增加盛有___(填 名称)溶液的洗气瓶。
探究二:热重法(TG)确定分解所得固体产物的组成
[数据分析]
称取3.60g草酸亚铁晶体( FeC2O4﹒2H2O,为相对分子质量为180),用热重法对其进行热分解,得到剩余固体的质量随温度变化的曲线如图所示。300°C时,剩余固体为纯净物且是铁的氧化物,通过计算确定该物质的化学式为_________。
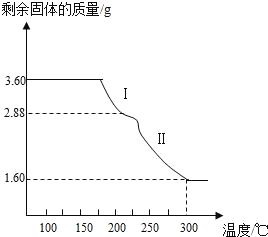
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C、D均为初中化学常见物质,已知A、C为化合物,B、D为单质。它们的转化关系如图所示(部分反应物、生成物和反应条件均已略去)。
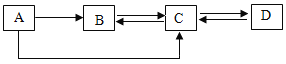
对于以上物质和转化关系,有下列说法:
(1)B与D在一定条件下能发生化学反应
(2)B→C既是氧化反应,也是化合反应
(3)A与C元素组成相同,化学性质相同
(4)B的相对分子质量大于D
以上说法正确的是( )
A.(1)(2)B.(1)(3)C.(1)(4)D.(2)(4)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com