
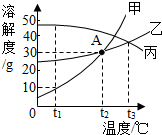
 甲、乙、丙三种固体物质的溶解度曲线如图所示.试据图回答下列问题:
甲、乙、丙三种固体物质的溶解度曲线如图所示.试据图回答下列问题:分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)通过分析溶解度曲线可知,t1℃时,甲、乙、丙三种物质的溶解度由大到小的关系为丙>乙>甲;
(2)A点含义为t1℃时,甲、乙物质的溶解度相等;
(3)t2℃时,甲物质的溶解度是30g,所以甲物质的饱和溶液中溶质与溶剂的质量比为3:10;
(4)甲物质的溶解度受温度影响变化较大,所以甲物质的饱和溶液中含有少量乙,要提纯甲可采取的方法是降温结晶;
(5)降低温度,丙物质会析出晶体,甲、乙物质不会析出晶体,但是t2℃丙物质的溶解度依然最大,所以将t1℃时甲、乙、丙三种物质的饱和溶液升高温度到t2℃(不考虑溶剂蒸发),三者溶质质量分数的大小关系为丙>乙>甲.
故答案为:(1)丙>乙>甲;
(2)t1℃时,甲、乙物质的溶解度相等;
(3)3:10;
(4)降温结晶;
(5)丙>乙>甲.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.


科目:初中化学 来源: 题型:选择题
| A. | 化合反应 | B. | 分解反应 | C. | 复分解反应 | D. | 置换反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
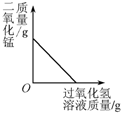 |  | 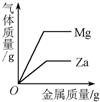 | 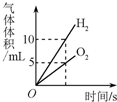 |
| A向一定量的二氧化锰中加入过氧化氢溶液 | B加热一定量的高锰酸钾固体 | C向两份完全相同的稀盐酸中分别加入锌粉、镁粉 | D将水通电电解一段时间 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
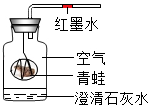 某同学为研究动物的呼吸作用,用如图所示的方式进行实验.实验过程中发现澄清石灰水变浑浊,红墨水向左(填“左”或“右”)移动,实验结束后将燃着的木条放到瓶中,木条熄灭.说明动物呼吸时吸进氧气气体,呼出二氧化碳气体.
某同学为研究动物的呼吸作用,用如图所示的方式进行实验.实验过程中发现澄清石灰水变浑浊,红墨水向左(填“左”或“右”)移动,实验结束后将燃着的木条放到瓶中,木条熄灭.说明动物呼吸时吸进氧气气体,呼出二氧化碳气体.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 三聚氰胺属于有机化合物 | |
| B. | C3H6N6中质量分数最高的元素是氮元素 | |
| C. | C3H6N6中各原子的原子个数比为1:2:2 | |
| D. | 一个三聚氰胺分子中含有3个氮原子 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
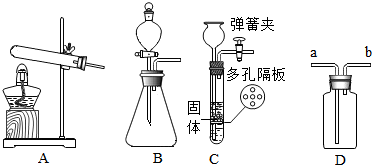 如图为实验室制取气体的一些常用装置.
如图为实验室制取气体的一些常用装置.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com