
| 1H £Ø1.008 | 2He £Ø4.003 | ||||||
| 3Li £Ø6.941 | 4Be £Ø9.01 | 5B £Ø10.81 | 6C £Ø12.01 | 7N £Ø14.01 | 8O £Ø16.00 | 9F £Ø19.00 | 10Ne £Ø20.18 |
| 11Na £Ø22.99 | 12Mg £Ø24.31 | 13Al £Ø26.98 | 14Si £Ø28.09 | 15P £Ø30.97 | 16S £Ø32.06 | 17Cl £Ø35.45 | 18Ar £Ø39.95 |
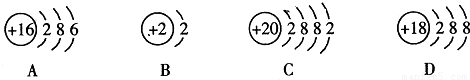
 CO+H2£®
CO+H2£® CO+H2£®
CO+H2£®


| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| µŚ1ÖÜĘŚ | 1H 1.008 |
2He 4.003 | ||||||
| µŚ2ÖÜĘŚ | 3Li 6.941 |
4Be 9.012 |
5B 10.81 |
6C 12.01 |
7N 14.01 |
8O 16.00 |
9F 19.00 |
10Ne 20.18 |
| µŚ3ÖÜĘŚ | 11Na 22.99 |
12Mg 24.31 |
13Al 26.98 |
14Si 28.09 |
15P 30.97 |
16S 32.06 |
17Cl 35.45 |
18Ar 39.95 |
 £¬µŚ3ÖÜĘŚÖŠÄ³ŌŖĖŲÓėŃõŌŖĖŲµÄ»ÆѧŠŌÖŹĻąĖĘ£¬øĆŌŖĖŲµÄŌ×Ó½į¹¹Ź¾ŅāĶ¼ĪŖ
£¬µŚ3ÖÜĘŚÖŠÄ³ŌŖĖŲÓėŃõŌŖĖŲµÄ»ÆѧŠŌÖŹĻąĖĘ£¬øĆŌŖĖŲµÄŌ×Ó½į¹¹Ź¾ŅāĶ¼ĪŖ  £¬Ōņx=
£¬Ōņx=²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
 ŌŖĖŲÖÜĘŚ±ķŹĒѧĻ°»ÆѧµÄÖŲŅŖ¹¤¾ß£¬Ķ¼ŹĒŌŖĖŲÖÜĘŚ±ķÖŠµÄŅ»øń£¬“ÓøĆĶ¼ÖŠ£¬ĪŅĆĒ»ńČ”µÄĻą¹ŲŠÅĻ¢ÖŠ“ķĪóµÄŹĒ£Ø””””£©
ŌŖĖŲÖÜĘŚ±ķŹĒѧĻ°»ÆѧµÄÖŲŅŖ¹¤¾ß£¬Ķ¼ŹĒŌŖĖŲÖÜĘŚ±ķÖŠµÄŅ»øń£¬“ÓøĆĶ¼ÖŠ£¬ĪŅĆĒ»ńČ”µÄĻą¹ŲŠÅĻ¢ÖŠ“ķĪóµÄŹĒ£Ø””””£©²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
 ŌŖĖŲÖÜĘŚ±ķŹĒѧĻ°»ÆѧµÄÖŲŅŖ¹¤¾ß£®ČēĶ¼ŹĒŌŖĖŲÖÜĘŚ±ķÖŠµÄŅ»øń£¬“ÓÖŠ»ńČ”µÄŠÅĻ¢“ķĪóµÄŹĒ£Ø””””£©
ŌŖĖŲÖÜĘŚ±ķŹĒѧĻ°»ÆѧµÄÖŲŅŖ¹¤¾ß£®ČēĶ¼ŹĒŌŖĖŲÖÜĘŚ±ķÖŠµÄŅ»øń£¬“ÓÖŠ»ńČ”µÄŠÅĻ¢“ķĪóµÄŹĒ£Ø””””£©²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ

²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com