
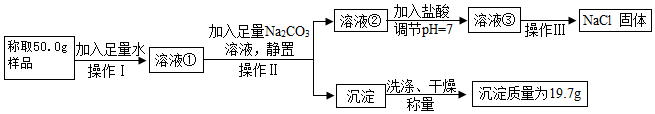
分析 (1)用托盘天平称量样品前对天平进行的第一步操作是调节零点;
(2)向溶液①中加入足量Na2CO3溶液的目的是使氯化钡完全反应;
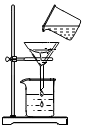
过滤时要注意操作注意事项;
(3)蒸发皿不属于玻璃仪器;
玻璃棒的用途有引流、搅拌、转移物质等;
(4)碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,根据反应的化学方程式及其提供的数据可以计算样品中氯化钠质量百分含量.
解答 解:(1)用托盘天平称量样品前对天平进行的第一步操作是调节零点.
故填:调节零点.
(2)向溶液①中加入足量Na2CO3溶液的目的是使氯化钡完全反应;
操作中存在的两处错误是:没有利用玻璃棒引流,漏斗下端没有紧贴烧杯壁.
故填:使氯化钡完全反应;没有利用玻璃棒引流;漏斗下端没有紧贴烧杯壁.
(3)a.过滤中用到的仪器有酒精灯、玻璃棒、蒸发皿等,其中蒸发皿不属于玻璃仪器,该选项说法不正确;
b.该操作中用玻璃棒不断搅拌的目的是防止局部温度过高,造成液滴飞溅,该选项说法正确;
c.当蒸发皿中出现较多固体时,停止加热,该选项说法正确;
d.停止加热后,不能立即将蒸发皿直接放在试验台上,以免烫坏试验台,该选项说法不正确.
故选:bc.
(4)设样品中氯化钡质量为x,
BaCl2+Na2CO3═BaCO3↓+2NaCl,
208 197
x 19.7g
$\frac{208}{x}$=$\frac{197}{19.7g}$,
x=20.8g,
样品中氯化钠质量百分含量为:$\frac{50.0g-20.8g}{50.0g}$×100%=58.4%,
故填:58.4%.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.


 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:初中化学 来源: 题型:实验探究题


查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 温度/℃ | 10 | 30 | 50 | 70 | 90 |
| 溶解度/g | 27.7 | 39.3 | 49.0 | 54.1 | 51.1 |
| A. | 硫酸镁的溶解度随温度升高而增大 | |
| B. | 10℃时,27.7g硫酸镁和72.3g水可配制成质量分数为27.7%的硫酸镁溶液 | |
| C. | 50℃时,100g的硫酸镁饱和溶液中溶质和溶剂的质量比为49:100 | |
| D. | 70℃时的硫酸镁饱和溶液升温至90℃,溶液的溶质质量分数增大 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 向烧杯中逐渐加入X溶液至过量(图甲),生成沉淀或气体的质量(纵坐标)与加入X溶液的质量(横坐标)关系不符合图乙的是( )
向烧杯中逐渐加入X溶液至过量(图甲),生成沉淀或气体的质量(纵坐标)与加入X溶液的质量(横坐标)关系不符合图乙的是( )| 烧杯中的物质 | X溶液 | |
| A | 稀硫酸 | 氯化钡溶液 |
| B | 氯化钠溶液 | 硝酸银溶液 |
| C | 硫酸和硫酸铜混合溶液 | 氢氧化钠溶液 |
| D | 碳酸氢钠溶液 | 稀盐酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 室温下的氯化钠饱和溶液不能再溶解氯化钾 | |
| B. | 取出部分上层溶液,可将接近饱和的氯化钠溶液变为饱和 | |
| C. | 可用硝酸银溶液鉴别氯化钠和氯化镁溶液 | |
| D. | 将100g质量分数为20%的氯化钠溶液稀释为10%,所用的仪器有:烧杯、量筒、玻璃棒和胶头滴管 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
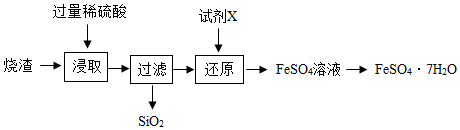
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 尿液4.7~8.4 | B. | 唾液6.6~7.1 | C. | 血浆7.35~7.45 | D. | 胃液0.9~1.5 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | X | O2 | CO2 | H2O |
| 反应前的质量/g | 19 | 34 | 6 | 2 |
| 反应后的质量/g | 11 | 待测 | 28 | 20 |
| A. | 表中的待测值为32 | B. | X中一定含有C、H、O元素 | ||
| C. | 该反应是置换反应 | D. | 反应中CO2和H2O的质量比为11:9 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
 某化学试剂乙酰丙酮(化学式:C5H8O2)的试剂标签如图:
某化学试剂乙酰丙酮(化学式:C5H8O2)的试剂标签如图:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com