
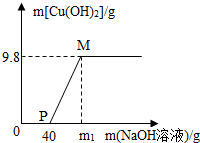
 向含CuCl2和HCl的100 克混合溶液中,逐滴加入溶质质量分数为10%的NaOH溶液200克,参加反应的NaOH溶液质量与生成沉淀Cu(OH)2质量关系如图,据图回答:
向含CuCl2和HCl的100 克混合溶液中,逐滴加入溶质质量分数为10%的NaOH溶液200克,参加反应的NaOH溶液质量与生成沉淀Cu(OH)2质量关系如图,据图回答:分析 (1)根据整个反应过程的生成物及反应物来判断
(2)已知氯化铜和氢氧化钠生成氢氧化铜沉淀的质量可求出反应的氢氧化钠的质量,盐酸和氯氧化钠反应消耗的氢氧化钠溶液质量为40g,可求出整个过程中消耗的氢氧化钠溶液的质量.
(3)M点溶液中的溶质是氯化钠,氯化钠有两部分,一是盐酸与氢氧化钠生成的,另一部分是氯化铜和氢氧化钠反应生成的.溶液质量可用质量守恒法来求,加入的混合溶液的总质量+氢氧化钠溶液的质量-生成的氢氧化铜沉淀的质量.从而求出溶液中溶质质量分数.
解答 解:(1)P点表示氯化氢和氢氧化钠恰好完全反应,此时氯化铜还没和氢氧化钠反应,故溶液中的溶质为NaCl CuCl2
(2)设生成9.8g氢氧化铜沉淀需氢氧化钠溶液的质量为x,生成氯化钠的质量为z
CuCl2+2NaOH═Cu(OH)2↓+2NaCl,
80 98 117
x×10% 9.8g z
$\frac{80}{x×10%}=\frac{98}{9.8g}=\frac{117}{z}$
x=80g z=11.7g
氯化氢和氢氧化钠反应时消耗的氢氧化钠溶液的质量为40g,所以m1=40g+80g=120g
(3)设氯化氢与氢氧化钠反应生成氯化钠的质量为y
NaOH+HCl═NaCl+H2O
40 58.5
40g×10% y
$\frac{40}{40g×10%}=\frac{58.5}{y}$
y=5.85g
M点溶液中的溶质氯化钠的质量为11.7g+5.85g=17.55g
M点溶液的溶质质量分数=$\frac{17.55g}{100g+120g-9.8g}$×100%≈8.3%
答:M点溶液的溶质质量分数为8.3%
故答案为:(1)NaCl和CuCl2.(2)120 (3)8.3%
点评 本题考查化学方程式与溶液的综合计算,解题关键是分析清楚反应过程的先后,找出每个过程中已知物质的质量.


科目:初中化学 来源: 题型:填空题
 某校化学兴趣小组对雪碧中的气体进行了如下探究,请你回答下列问题:
某校化学兴趣小组对雪碧中的气体进行了如下探究,请你回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 二氧化碳可以用来做灭火剂、制冷剂 | |
| B. | CO2可作为气体肥料 | |
| C. | 二氧化碳没有毒性,不会导致人类死亡 | |
| D. | 二氧化碳可做为大气中氧气的来源 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 2eF+6HCl═2Fel3C+3H2↑ | B. | Cu+H2SO4═CuSO4+H2↑ | ||
| C. | Fe+O2$\frac{\underline{\;点燃\;}}{\;}$Fe304 | D. | Mg+2HCl═MgCl2+H2↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  水的电解 水的电解 | |
| B. |  一定温度下,不饱和氯化钠溶液中加入氯化钠 一定温度下,不饱和氯化钠溶液中加入氯化钠 | |
| C. |  足量的镁粉和铁粉,分别放入质量和质量分数相同的稀盐酸中 足量的镁粉和铁粉,分别放入质量和质量分数相同的稀盐酸中 | |
| D. |  用等质量、等浓度的双氧水分别制取氧气 用等质量、等浓度的双氧水分别制取氧气 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com