
分析 ①根据分子中碳、氢原子个数呈一定的规律分析.
②根据单质中元素的化合价为0、在化合物中正负化合价代数和为零,分别计算各物质中氯元素的化合价,得出化合价的排列规律,进行分析解答即可.
解答 解:①根据化学式可以发现随着化学式中碳原子的个数增加,氢原子的个数也在增加,并且每增加1个碳原子同时增加2个氢原子,所以C2H4、C3H6、C4H8、所以空格处应为C5H10,
②钠元素显+1价,设NaCl中氯元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x=0,则x=-1价.
钠元素显+1价,氧元素显-2价,设NaClO中氯元素的化合价是y,根据在化合物中正负化合价代数和为零,可得:(+1)+y+(-2)=0,则y=+1价.
钾元素显+1价,氧元素显-2价,设KClO3中氯元素的化合价是z,根据在化合物中正负化合价代数和为零,可得:(+1)+x+(-2)×3=0,则z=+5价.
氢元素显+1价,氧元素显-2价,设HClO4中氯元素的化合价是w,根据在化合物中正负化合价代数和为零,可得:(+1)+w+(-2)×4=0,则w=+7价.
则氯元素的化合价是按照从低到高的顺序排列的,所以空格中氯元素的化合价为在-1到+1之间.根据单质中元素的化合价为0,Cl2属于单质,故氯元素的化合价为0.
故答案为:①C5H10,②Cl2.
点评 本题难度有一定难度,找到化学式中隐藏的规律是正确解答本题的关键.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
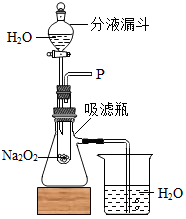 在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小军很感兴趣,于是,他和同学们进行探究.
在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小军很感兴趣,于是,他和同学们进行探究.查看答案和解析>>
科目:初中化学 来源: 题型:推断题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
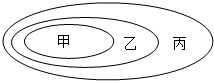 图中甲、乙、丙三个椭圆分别代表某个概念或某类物质.下列能构成图示关系的是( )
图中甲、乙、丙三个椭圆分别代表某个概念或某类物质.下列能构成图示关系的是( )| A. | 甲是杠杆、乙是滑轮、丙是简单机械 | |
| B. | 甲是动能、乙是势能、丙是机械能 | |
| C. | 甲是碱、乙是化合物、丙是纯净物 | |
| D. | 甲是化合反应、乙是分解反应、丙是置换反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
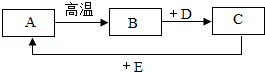
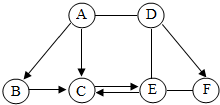 如图 A、B、C、D、E、F为初中化学常见的六种含氧化合物,A、B、C 均由两种元素组成,在常温下状态各不相同,其中A为红色粉末,D、E、F 均由三种元素组成,且物质类别各不相同.“→”表示物质间的转化关系,“-”表示两种物质能相互反应(部分反应物、生成物及反应条件未标出).回答下列问题:
如图 A、B、C、D、E、F为初中化学常见的六种含氧化合物,A、B、C 均由两种元素组成,在常温下状态各不相同,其中A为红色粉末,D、E、F 均由三种元素组成,且物质类别各不相同.“→”表示物质间的转化关系,“-”表示两种物质能相互反应(部分反应物、生成物及反应条件未标出).回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com