
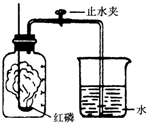
 某同学设计了测定空气中氧气含量的实验,实验装置如图,实验步骤如下:
某同学设计了测定空气中氧气含量的实验,实验装置如图,实验步骤如下:分析 实验的目的是测定空气中氧气含量,原理是消耗氧气使装置内外产生压强差,水被吸入占据氧气的空间,从而达到测定氧气的目的.
(1)根据该实验注意事项分析;
(2)根据红磷的燃烧结合压强知识分析,红磷与氧气反应生成固体,消耗了瓶内的气体,压强减小,外界大气压会压着水进入集气瓶;根据实验现象分析;
(3)在该实验中,剩余的气体主要是氮气;
(4)根据红磷燃烧生成五氧化二磷固体解答;
(5)木炭和氧气反应又生成二氧化碳,没有改变集气瓶内的压强;
(6)如果操作不当,会影响实验结果,甚至会导致实验失败.
解答 解:(1)实验的目的是测定空气中氧气含量,原理是消耗氧气使装置内外产生压强差,水被吸入占据氧气的空间,从而达到测定氧气的目的,红磷过量,可使集气瓶中的氧气完全消耗.
(2)步骤②集气瓶中的现象是 剧烈燃烧,发黄光,产生大量白烟,放热,步骤③中打开止水夹的现象是烧杯中的水倒流至集气瓶,液面上升在一等分刻度处,由此得出的结论是:空气中氧气的体积分数约为五分之一;
(3)剩余的气体主要是氮气,水进入瓶内占五分之一,不再继续进入,说明氮气不能与红磷反应,也不能溶于水或与水反应;则该实验可推断出氮气 难溶于水和其化学性质 不活泼的结论.
(4)红磷燃烧生成五氧化二磷固体,反应的化学方程式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;其反应的文字表达式是:红磷+氧气$\stackrel{点燃}{→}$五氧化二磷;
(5)测定空气中氧气的体积分数利用的是压强的改变,所以若把红磷换成木炭,木炭和氧气反应又生成二氧化碳,没有改变集气瓶内的压强,达不到实验目的.
(6)装置漏气,都能够导致测定的空气体积分数小于五分之一.
故答案为:
(1)确保集气瓶内的氧气消耗尽;
(2)剧烈燃烧,发黄光,产生大量白烟,放热;烧杯中的水倒流至集气瓶,液面上升在一等分刻度处;$\frac{1}{5}$;
(3)难;不活泼;
(4)红磷+氧气$\stackrel{点燃}{→}$五氧化二磷(4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5)
(5)否,木炭和氧气反应又生成二氧化碳,没有改变集气瓶内的压强,达不到实验目的.
(6)装置漏气,红磷不足,没有冷却至室温就打开弹簧夹.
点评 熟记用红磷测定空气里氧气含量的实验原理、操作步骤、实验现象、实验结论和注意事项是解答这类题目的基础.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 2CO──2个一氧化碳分子 | B. | Mg+2──1个镁离子 | ||
| C. | H2──2个氢原子 | D. | $\stackrel{+2}{Cu}$O──铜元素的化合价为+2价 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com