

分析 (一)铁能和胃液中的稀盐酸反应生成氯化亚铁和氢气;
(二)铁和水、氧气同时接触时容易生锈,氯化钠溶液能够促进铁生锈;
铁和水、氧气反应生成氢氧化亚铁;
凡是有气体参加或产生的实验,实验前一定要检查装置的气密性,以防装置漏气影响实验结果;
氢氧化钠溶液能够吸收二氧化碳,并且能和二氧化碳反应生成碳酸钠和水;
根据装置中的质量变化情况可以进行相关方面的计算;
碱石灰能够吸收水蒸气和二氧化碳;
(三)高温条件下,氧化铁和一氧化碳反应生成铁和二氧化碳;
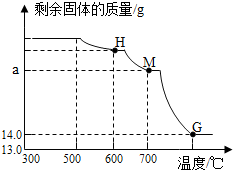
图中M点对应的a点是反应生成氧化亚铁的质量.
解答 解:(一)铁和稀盐酸反应的化学方程式为:Fe+2HCl═FeCl2+H2↑.
故填:Fe+2HCl═FeCl2+H2↑.
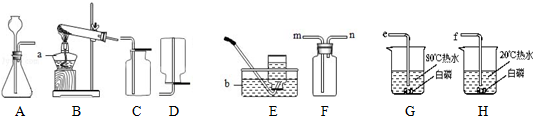
(二)(1)如图为某兴趣小组探究铁生锈的三个实验,最先观察到铁锈的是C,这是因为氯化钠溶液能够促进铁生锈.
故填:C.
(2)Fe→Fe(OH)2反应的化学方程式为:2Fe+O2+2H2O=2Fe(OH)2.
故填:2Fe+O2+2H2O=2Fe(OH)2.
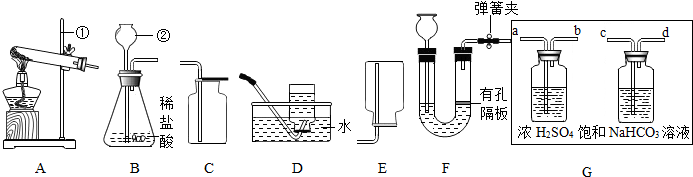
(3)①装配好实验装置后,首先要检查装置气密性.
故填:检查装置气密性.
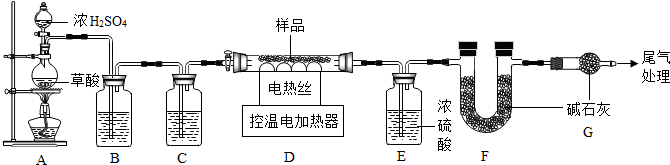
②通过B、C装置可得到干燥、纯净的CO气体,洗气瓶B中应盛放氢氧化钠溶液,用来吸收二氧化碳气体.
故填:c.
③设碳酸亚铁质量为m,
装置F增重2.2g,说明碳酸亚铁分解生成了2.2g二氧化碳,装置E增重3.6g,说明铁锈中的结晶水的质量是3.6g,
FeCO3$\frac{\underline{\;\;△\;\;}}{\;}$FeO+CO2↑,
116 44
m 2.2g
$\frac{116}{x}$=$\frac{44}{2.2g}$,
x=5.8g,
铁锈中氧化铁质量为:25.4g-5.8g-3.6g=16g,
根据题意有:16g:3.6g=160:18x,
x=2.
故填:5.8;2.
④若缺少G装置,空气中的水蒸气和二氧化碳会进入F中,导致二氧化碳质量偏大,从而导致测得的碳酸亚铁质量偏大;
碳酸亚铁质量偏大时,会导致计算的氧化铁质量偏小,从而导致测定的x值偏大.
故填:偏大;偏大.
(三)(1)写出工业上用赤铁矿(主要成分Fe2O3)炼铁主要原理的化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
故填:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)图中M点对应的a点是反应生成氧化亚铁的质量,铁锈中铁元素质量为:5.8g×$\frac{56}{116}$×100%+16g×$\frac{112}{160}$×100%=14g,则生成氧化亚铜质量为:
14g÷($\frac{56}{72}$×100%)=18g,
图中M点对应的a=18.
故填:18.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 二氧化锰和硫酸铜溶液都可作为过氧化氢分解的催化剂.在一节化学实验课上,小花同学向10g过氧化氢中加入1.65g溶质质量分数为10%的硫酸铜溶液.实验过程中溶液总质量与反应时间的关系如图所示.求:
二氧化锰和硫酸铜溶液都可作为过氧化氢分解的催化剂.在一节化学实验课上,小花同学向10g过氧化氢中加入1.65g溶质质量分数为10%的硫酸铜溶液.实验过程中溶液总质量与反应时间的关系如图所示.求:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质 | 加入的试剂和操作 |
| A | O2(CO2) | 通过灼热的铜网 |
| B | CaCO3(CaO) | 高温煅烧 |
| C | Cu(NO3)2溶液(AgNO3) | 足量铜粉,过滤 |
| D | CO2(CO) | 空气,点燃 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
物质 |  |  |  |  |
| 化学式 | NaCl | C | ③NaHCO3 | CaO④CaO |
| 用途 | ①做调味品、生理盐水、选种、化工原料、消除积雪等 | ②切割大理石、做装饰品(钻石)等 | 做发酵粉 | 做干燥剂 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com