
下列鉴别两种不同物质的方法,错误的是( )
选项 | 待鉴别的物质 | 鉴别方法 |
A | CO2与O2 | 燃着的木条,观察木条燃烧情况 |
B | 棉线与羊毛线 | 点燃,闻产生的气味,观察生成的灰烬 |
C | AgCl与NaCl | 加水,观察是否溶解 |
D | NaOH与Na2CO3 | 溶于水,滴加酚酞试液,观察溶液的颜色变化 |
A. A B. B C. C D. D
科目:初中化学 来源:2020年重庆市指标到校化学试卷 题型:单选题
在一定条件下, 甲、 乙、丙、丁四种物质在密闭容器中反应,测得反应前后各物质的质量分数如图所示。下列说法正确的是()
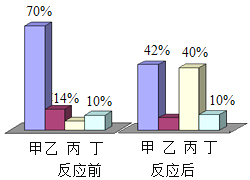
A.丁是该反应的催化剂
B.该反应的基本类型为分解反应
C.该反应中乙、丙的质量比为3:17
D.该反应中甲、丙的质量比为7:10
查看答案和解析>>
科目:初中化学 来源:2020年天津市河西区中考二模化学试卷 题型:填空题
在宏观、微观和符号之间建立联系是化学特有的思维方式。
(1)根据以下几种粒子的结构示意图,回答下列问题。
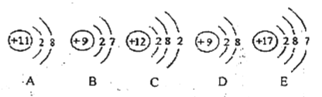
①属于同种元素的粒子是_____(填序号,下同);
②具有相对稳定结构的粒子是_____;
③B在元素周期表中排在第_____周期。
④B和E两种原子的_____相同,所以它们具有相似的化学性质。
(2)我国科学家成功合成新型催化剂,能将CO2高效转化为甲醇(CH3OH)。该化学反应的微观过程如下图所示。
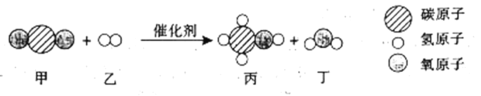
①反应前后,______(填“分子”或“原子”)的种类不变。
②反应的生成物质量比为______。
查看答案和解析>>
科目:初中化学 来源:2020年福建省泉州市洛江区中考模拟化学试卷 题型:推断题
从化合价和物质类别两个维度认识元素及其化合物性质是重要的化学学习方式。下图是Fe及其化合物的化合价——物质类别二维图。
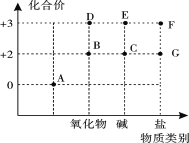
(知识卡片):
在化学反应中有元素化合价升高,则必有元素化合价降低,且化合价升高的总数一定等于化合价降低的总数。
请回答下列问题:
(1)A物质所属物质类别是_____。
(2)B的化学式是_____。
(3)工业上可以用_____(填物质名称)和D在高温下反应生产A。
(4)G可以是硫酸盐,这种硫酸盐可用作_____病人的治疗药物之一、
(5)C在潮湿的空气中很容易发生化合反应变成E,该反应的化学方程式是_____。
(6)高铁酸钾(K2FeO4)是常用的自来水消毒剂,高铁酸钾中铁的化合价为_____。
查看答案和解析>>
科目:初中化学 来源:2020年福建省泉州市洛江区中考模拟化学试卷 题型:单选题
下列图示的实验操作中正确的是( )
A.  点燃酒精灯 B.
点燃酒精灯 B.  稀释浓硫酸
稀释浓硫酸
C.  测溶液的pH D.
测溶液的pH D. 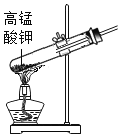 制取氧气
制取氧气
查看答案和解析>>
科目:初中化学 来源:2020年山东省济南市区中考二模化学试卷 题型:填空题
(1)铁是生产、生活中使用最广泛的一种金属。
①现在的中国高铁与轨道交通已经成为了中国一张全新的名 片,中国的高铁出口也正在引领着世界铁路变革。钢轨属于_____(填“单质”“合金”“氧化物”之一)。

②碳化铁(Fe3C)在冶金上称为渗碳体,可由铁粉渗碳来制得。它有优良的切削加工性能,广泛用于机械制造。碳化铁在足量的空气中高温煅烧,生成四氧化三铁和能使澄清石灰水变浑浊的气体,该反应的化学方程式为_____。
(2)我国著名化学家侯德榜创立的侯氏制碱法,是以海水“晒盐”得到的氯化钠为原料, 同时制得 Na2CO3 和 NH4Cl 产品。Na2CO3 和 NH4Cl 的溶解度曲线如图所示。

试回答下列问题:
①t2℃时,Na2CO3溶液的溶质质量分数_____NH4Cl 溶液的溶质质量分数(填“大于”“等于”“小于”“无法判断” 之一)。
②将t2℃时等质量的Na2CO3 和NH4Cl 的饱和溶液均降温至t1℃时,Na2CO3 溶液的溶质质量分数_____NH4Cl 溶液的溶质质量分数(填“大于”“等于”“小于”“无法判断”之一)。
③若Na2CO3 固体中含少量NH4Cl,提纯Na2CO3 可采用_(填“蒸发结晶” 或“降温结晶”之一)的方法。
查看答案和解析>>
科目:初中化学 来源:广东省茂名市高州市七校2019-2020学年九年级下学期4月联考化学试卷 题型:计算题
某食用碱的主要成分是Na2CO3,其中含有少量的NaCl,小明同学为测定该食用碱中Na2CO3的质量分数,他进行了以下实验,取40 g食用碱,加水配成400g的溶液,把溶液平均分为四份,然后分别加入一定质量分数的CaCl2溶液,实验数据见下表:
实验一 | 实验二 | 实验三 | 实验四 | |
食用碱溶液的质量 | 100g | 100g | 100g | 100g |
加入CaCl2溶液的质量 | 20g | 40g | 60g | 80g |
生成沉淀的质量 | 2.5g | 5g | m | 8g |
请分析表中数据并计算回答。
(1)m=________;
(2)40 g该食用碱配成的溶液与足量CaCl2溶液反应,最多生成沉淀质量为多少;
(3)该食用碱中Na2CO3的质量分数是?(写出计算过程,答案精确到0.1%)
(4)请根据实验四的数据画图并标上合适的坐标。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com