
| A.酸中一定含有氢元素 |
| B.呈碱性的溶液一定是碱的溶液 |
| C.生成盐和水的反应一定是中和反应 |
| D.在化学反应中,质量和化学性质都不改变的物质一定是催化剂 |
科目:初中化学 来源:不详 题型:推断题
| 加入物质 | 碳酸钠溶液 | 硝酸银溶液 | 稀盐酸 |
| 现 象 | 产生白色沉淀 | 产生白色沉淀 | 固体溶解 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
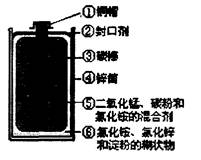
| A.滤纸破损 | B.过滤过程中滤液的液面超过了滤纸的边缘 |
| C.烧杯不干净 | D.滤液C中的物质相互反应 |
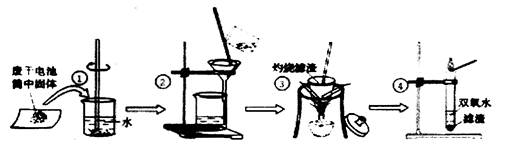
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题
| 20℃时,一些物质的溶解度 | ||
| | OH- | CO32- |
| Na+ | 溶 | 溶 |
| Ca2+ | 微 | 不 |
| Mg2+ | 不 | 微 |

| 物质 | NaCl | NaHCO3 | NH4Cl | NH3 | CO2 |
| 溶解度 | 36.0g | 9.6g | 37.2g | 710 | 0.9 |

查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.淀粉和葡萄糖(加水,振荡) | B.硬水与软水(加肥皂水,振荡) |
| C.蒸馏水与盐水(过滤) | D.白酒和食醋(闻气味) |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.“食盐”不是盐 | B.“纯碱”不是碱 |
| C.“水银”不是银 | D.“干冰”不是冰 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:实验题

| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度g | 36 | 109 | 215 | 9.6 |
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中,滴加 | 产生大量的气泡 | 该溶液是 ,反应的化学方程式 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.生石灰--氢氧化钙--Ca(OH)2 | B.纯碱--氢氧化钠--NaOH |
| C.碳铵--碳酸铵--NH4HCO3 | D.小苏打--碳酸氢钠--NaHCO3 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:推断题
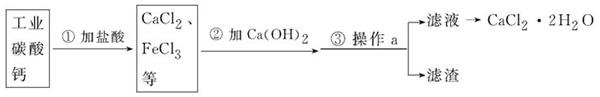
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com