
| 物质 | 酒精 | 氧气 | 水 | 二氧化碳 | X |
| 反应前质量/g | 4.6 | 8.0 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 5.4 | 4.4 | a |
| A. | X一定不是催化剂 | |
| B. | 酒精和氧气的计量数之比为1:3 | |
| C. | X是一氧化碳 | |
| D. | 若起始时氧气的质量≥9.6g,则无X生成 |
分析 根据质量守恒定律,由物质质量的增减量可确定反应物和生成物的质量,从而得出a的值,再根据物质的化学式和物质的质量可确定X的元素组成.
解答 解:A、由表中数据分析可知,反应前后,乙醇的质量减少了4.6g,故乙醇是反应物,参加反应的乙醇的质量为4.6g;同理可以确定氧气是反应物,参加反应的氧气的质量为8.0g;水是生成物,生成的水的质量为5.4g;生成二氧化碳的质量为4.4g;由质量守恒定律,X应是生成物,且生成的X的质量为4.6g+8.0g-5.4g-4.4g=2.8g,故表中a的值为为0g+2.8g=2.8g,X的质量增加,故一定不是该反应的催化剂;故选项说法正确.
B、由A选项分析可知,酒精和氧气的计量数之比为$\frac{4.6g}{46}:\frac{8.0g}{16}$=1:5,故选项说法错误.
C、根据反应前后元素质量不变,反应物乙醇中含氢元素的质量为4.6g×$\frac{1×6}{12×2+1×6+16}$×100%=0.6g,其中氧元素的质量为:4.6g×$\frac{16}{12×2+1×6+16}$×100%=1.6g,碳元素的质量为4.6g-1.6g-0.6g=2.4g;生成物水中含氢元素的质量为5.4g×$\frac{1×2}{1×2+16}$×100%=0.6g,其中氧元素的质量为5.4g-0.6g=4.8g;生成物二氧化碳中含碳元素的质量为:4.4g×$\frac{12}{12+16×2}$×100%=1.2g,其中含有氧元素为4.4g-1.2g=3.2g;所以氢元素的质量相等,故X中不含氢元素,含碳元素为:2.4g-1.2g=1.2g,氧元素为:1.6g+8.0g-4.8g-3.2g=1.6g,故X中碳原子和氧原子的原子个数比为:$\frac{1.2g}{12}:\frac{1.6g}{16}$=1:1.故该物质是一氧化碳,故正确;
D、根据乙醇燃烧的方程式可知,4.6克乙醇能与9.6克的氧气恰好完全反应,生成了二氧化碳和水;故选项说法正确.
故选B.
点评 本题难度不大,考查的是质量守恒定律的应用,解题的关键是分析表中数据,灵活运用质量守恒定律.


 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CuSO4 Ca(NO3)2 | B. | AgNO3 K2CO3 | ||
| C. | Ba(OH)2 H2SO4 | D. | Na2CO3 HNO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
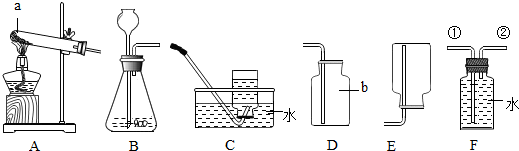

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水电解产生氢气和氧气,说明水分子中含有氢分子和氧分子 | |
| B. | 水通电分解和水的蒸发都是化学变化 | |
| C. | 水分子保持水的化学性质 | |
| D. | 在电解水的过程中,氢原子和氧原子发生变化 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com