
| A. | 物理性质 | B. | 化学性质 | C. | 制法 | D. | 用途 |
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| 序号 | 物质 | 杂质 | 方法 |
| A | 盐酸 | 硫酸 | 加入氢氧化钡溶液然后过滤 |
| B | 氧化钙 | 碳酸钙 | 加入适量的稀盐酸然后过滤 |
| C | 二氧化碳 | 水蒸气 | 把混合气体通过装有浓硫酸的洗气瓶 |
| D | 铜 | 铁 | 加入适量的氯化钙溶液然后过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
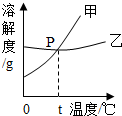 如表是NaCl和KNO3在不同温度时的溶解度,其变化趋势如图所示,下列推理合理的是( )
如表是NaCl和KNO3在不同温度时的溶解度,其变化趋势如图所示,下列推理合理的是( )| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶解度/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
| A. | 100g水里最多能溶解KNO331.6g | |
| B. | 表示NaCl的溶解度曲线是甲 | |
| C. | 温度t的范围可能在20℃-30℃之间 | |
| D. | 不饱和溶液变为饱和溶液,溶质的质量分数增大 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
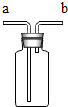 科学家发现,海底可燃冰分布的范围约占海洋总面积的10%,其储量是煤、石油和天然气总和的两倍,是迄今为止发现的海底最具价值的矿产资源.可燃冰也称为“甲烷水合物”.“置换法”是开采可燃冰设想方案之一,即将CO2注入海底的甲烷水合物储层,CO2较甲烷更易形成水合物,因而就能将甲烷水合物中的甲烷分子“挤走”,从而将其“置换”出来(原理:CH4•nH2O+CO2═CO2•nH2O+CH4).
科学家发现,海底可燃冰分布的范围约占海洋总面积的10%,其储量是煤、石油和天然气总和的两倍,是迄今为止发现的海底最具价值的矿产资源.可燃冰也称为“甲烷水合物”.“置换法”是开采可燃冰设想方案之一,即将CO2注入海底的甲烷水合物储层,CO2较甲烷更易形成水合物,因而就能将甲烷水合物中的甲烷分子“挤走”,从而将其“置换”出来(原理:CH4•nH2O+CO2═CO2•nH2O+CH4).查看答案和解析>>
科目:初中化学 来源: 题型:推断题
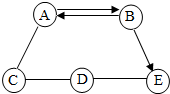 A、B、C、D、E为初中化学常见的五种物质,它们之间存在如图所示的关系(“→”表示物质经一步反应可转化为另一种物质,“-”表示相连两物质能发生化学反应,部分反应物、生成物及反应条件已略去).请回答下列问题:
A、B、C、D、E为初中化学常见的五种物质,它们之间存在如图所示的关系(“→”表示物质经一步反应可转化为另一种物质,“-”表示相连两物质能发生化学反应,部分反应物、生成物及反应条件已略去).请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验编号 | a1 | a2 | a3 | b1 | b2 | b3 | c1 | c2 | c3 |
| 溶质质量分数 | 2% | 2% | 2% | 6% | 6% | 6% | 10% | 10% | 10% |
| 水的温度(℃) | 20 | 40 | 60 | 20 | 50 | 60 | 20 | 40 | 70 |
| 溶液pH | 10.90 | 11.18 | 11.26 | 11.08 | 11.27 | 11.30 | 11.22 | 11.46 | 11.50 |
| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 |
| 溶液pH | 11.22 | 11.35 | 11.46 | 11.48 | 11.50 | 11.50 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | -2 | B. | -1 | C. | +1 | D. | +2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com