
 如图是小华同学在某食品包装袋内发现的一包干燥剂上的部分内容,该同学对干燥剂的成分进行了如下探究:
如图是小华同学在某食品包装袋内发现的一包干燥剂上的部分内容,该同学对干燥剂的成分进行了如下探究:

 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:初中化学 来源: 题型:
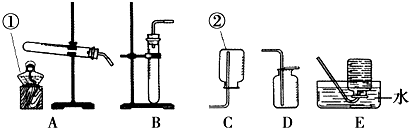
 如图所示,这是一瓶用排水法收集的一瓶无色气体.
如图所示,这是一瓶用排水法收集的一瓶无色气体.| 假设与猜想 | 实验方法及现象 | 结论 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
 材料一:近期天凉,流感病人越来越多了,为了预防该病毒,我们可用84消毒液进行消毒.
材料一:近期天凉,流感病人越来越多了,为了预防该病毒,我们可用84消毒液进行消毒. 查看答案和解析>>
科目:初中化学 来源: 题型:
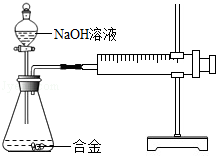 合金在生活中应用十分广泛.已知某合金粉末除含铝外,还含有铁、铜中的一种或两种.小明利用如图装置对合金粉末中铁、铜的存在进行探究时,误把氢氧化钠溶液当成稀硫酸加入到锥形瓶中,他惊奇的发现有无色气体放出,注射器活塞向右移动.
合金在生活中应用十分广泛.已知某合金粉末除含铝外,还含有铁、铜中的一种或两种.小明利用如图装置对合金粉末中铁、铜的存在进行探究时,误把氢氧化钠溶液当成稀硫酸加入到锥形瓶中,他惊奇的发现有无色气体放出,注射器活塞向右移动.| 实验步骤 | 实验现象 | 结论 |
| ①取一定量的合金粉末,加过量的 |
粉末部分溶解,并有无色气体放出. | 合金中一定含有 |
| ②取步骤①所得滤渣,加过量的 |
滤渣部分溶解,并有无色气体放出,溶液呈浅绿色. | 合金中一定含有 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com