
| 实验编号 | 硫酸的质量分数(均取20mL) | 锌的形状(均取1g) | 氢气的体积(mL)(均收集3min) |
| ① | 20% | 锌粒 | 31.7 |
| ② | 20% | 锌片 | 50.9 |
| ③ | 30% | 锌粒 | 61.7 |
| ④ | 30% | 锌片 | 79.9 |
| 时段(均为1分钟) | 第1分钟 | 第2分钟 | 第3分钟 | 第4分钟 | 第5分钟 | 第6分钟 |
| H2的体积 | 3.1mL | 16.7mL | 11.9mL | 9.6mL | 7.6mL | 6.0mL |


科目:初中化学 来源: 题型:
| A、氮气 | B、水蒸气 |
| C、稀有气体 | D、二氧化碳 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、氧气能支持燃烧,所以可作燃料 |
| B、氮气的化学性质比较稳定,所以可作焊接金属时的保护气 |
| C、二氧化碳本身不燃烧,也不支持燃烧,且密度大于空气,所以可用来灭火 |
| D、稀有气体在通电时能发出不同颜色的光,所以可用来制霓红灯 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
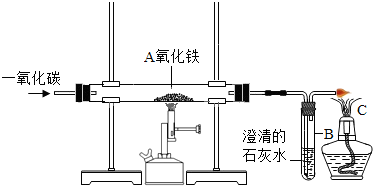
查看答案和解析>>
科目:初中化学 来源: 题型:
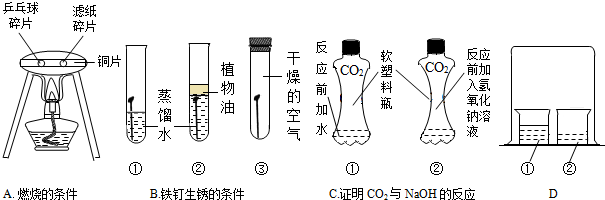
查看答案和解析>>
科目:初中化学 来源: 题型:
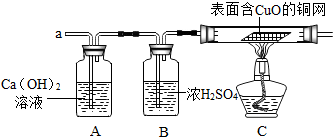 我省一燃烧厂制得的水煤气中可能含有一氧化碳、二氧化碳、氢气等气体,某化学兴趣实验小组同学用气囊装了一些回实验室进行鉴定.
我省一燃烧厂制得的水煤气中可能含有一氧化碳、二氧化碳、氢气等气体,某化学兴趣实验小组同学用气囊装了一些回实验室进行鉴定.查看答案和解析>>
科目:初中化学 来源: 题型:
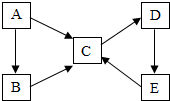 A、B、C、D、E均为初中化学常见物质,它们之间的转化关系如图所示:(“→”表示某一种物质经一步反应可转化为另一种物质,部分生成物及反应条件己略去),已知B、C的组成元素相同,D为一种常见的盐.
A、B、C、D、E均为初中化学常见物质,它们之间的转化关系如图所示:(“→”表示某一种物质经一步反应可转化为另一种物质,部分生成物及反应条件己略去),已知B、C的组成元素相同,D为一种常见的盐.查看答案和解析>>
科目:初中化学 来源: 题型:
| 步骤一 | 步骤二 | 步骤三 | 步骤四 | |
| 操作 | 取碳酸钠少量溶于水往溶液中滴加无色酚酞,把溶液分成三份, | 取上述滴有酚酞的溶液中滴加一定量的稀盐酸 | 取另一份溶液滴加澄清石灰水 | 取最后一份溶液滴加氯化钙溶液 |
| 现象 | 溶液变红 | 红色消失,产生气泡 | (3)溶液变浑浊,溶液呈 |
溶液变浑浊,红色退去 |
| 结论 | 碳酸钠溶液呈碱性 | 碳酸钠能与酸反应 | 碳酸钠能与碱反应 | 碳酸钠能与盐反应 |
| 反思 | (1)盐溶液 |
(2)反应后的溶液中溶质是 |
(4)由步骤三四可知确定久置的氢氧化钠的成分应滴加 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com