
【题目】在实验室里,某同学看到氢氧化钠试剂瓶的瓶口有白色粉末,他对白色粉末的成分作出了一些猜测。
猜测一:可能是氧氧化钠 猜测二:可能是碳酸钠 猜测三:可能是氧氧化钠和碳酸钠
为探究白色粉末的成分,他将该粉末溶于水,得到无色溶液,再迸行了如下实验:
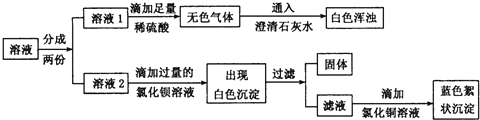
(1)根据实验现象推测,无色气体是________。
(2)在溶液2中滴加过量氯化钡溶液的目的是____________________
(3)由实验现象可知,猜测___是正确的,写出产生蓝色絮状沉淀的化学方程式__________________。
 天天向上口算本系列答案
天天向上口算本系列答案科目:初中化学 来源: 题型:
【题目】金属在日常生活,工农业生产和科学研究方面应用广泛。
(1)铜可用来制作导线,是因为其具有良好的延展性和__________。
(2)在空气中,铝表面生成一层致密的氧化膜,氧化膜的主要成分是_________。
(3)我国古代掌握了多种金属冶炼技术。春秋时期,发明了冶铁技术,其方法是将赤铁矿(主要成分为Fe2O3)与木炭交错堆积,利用自然风力进行燃烧,木炭不完全燃烧产生的CO将矿石中的Fe2O3还原成铁, 下图为铁制品循环利用的示意图
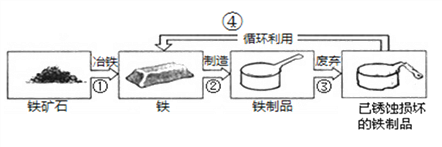
从“①”、“②”、“③”、“④”中,选出一定发生化学变化的是__________(填序号)不能用铁制容器盛放硫酸铜溶液的原因是______________________(用化学方程式表示)废旧金属“循环利用”的意义是_______________________(写一点即可)
(4)2015年,海昏侯墓出土了大量的青铜器,其表面有绿色的铜锈,其主要成分为碱式碳酸铜[Cu2(OH)2CO3]。试推测铜生锈是铜与氧气、水、_______共同作用的结果。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】城市生活垃圾的处理是世界性难题,某垃圾处理厂对生活垃圾进行处理与综合 利用部分流程如下:
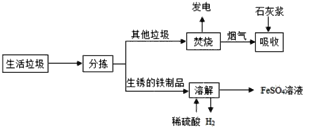
资料 1:垃圾焚烧产生的烟气中含有 SO2、HCl 等有害气体。 资料 2:+2 价的铁元素容易被空气中的氧气氧化。
资料 3:Fe 与 Fe2(SO4)3 反应生成 FeSO4。 回答下列问题:
(1)发电厂是利用垃圾焚烧产生的_____转变成电能;
(2)写出吸收步骤中属于中和反应的化学方程式_____;
(3)溶解步骤中,生锈的铁制品在足量的稀硫酸中充分反应后有黑色固体剩余,其主要成分是_____(写化学式);
(4)将所得硫酸亚铁溶液在氮气环境中加热蒸发浓缩、冷却结晶、过滤,得到硫酸亚铁晶体,其中氮气的作用是_____;
(5)请你就合肥市生活垃圾处理提一条建议_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】催化剂是指在化学反应中能够改变其它物质的化学反应速率,而本身的质量和化学性质在反应前后都没有改变的物质。某同学为了验证氧化铜(难溶于水)是否能做过氧化氢(H2O2)分解制取氧气的催化剂,设计实验如下:
【实验一】实验目的:探究氧化铜是否能改变过氧化氢分解的速率。
1.在试管中加入2ml 5%的过氧化氢溶液,将带火星的木条伸入试管中,观察现象。 | 1.带火星的木条没有明显变化 |
2. | 2. |
实验一结论:氧化铜能加快过氧化氢的分解速率
【实验二】实验目的:
实验步骤 | 实验现象 |
待实验一第2步的试管中没有气泡时,重新加入2ml过氧化氢溶液,观察现象。 |
实验二结论:氧化铜的化学性质在化学反应前后没有发生改变。
【实验三】实验目的:探究氧化铜的质量在化学反应前后有没有改变
在实验后,该同学将反应剩余物过滤、洗涤、干燥,再称量。得到黑色固体质量为1g。
实验三结论:氧化铜的质量在化学反应前后没有发生改变。
【实验结论】综上所述,说明了氧化铜是过氧化氢溶液分解的催化剂。
请写出该实验中过氧化氢溶液分解的化学反应方程式:
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是某反应的微观示意图,下列说法不正确的是( )
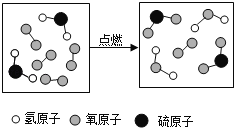
A.反应物中有单质
B.该反应为置换反应
C.生成物的分子个数比为1:1
D.参加反应的![]() 和
和![]() 的质量比为17:24
的质量比为17:24
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知:反应①是实验室制取气体A的常用方法,D常用来改良酸性土壤,它们之间的转化关系如下图所示(部分物质和反应条件已略去)。
![]()
图示关系中未涉及的基本反应类型为________;化学方程式①为________________________________;②B在生产或生活中的一种用途是________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是某硫酸试剂瓶标签上的部分文字说明。
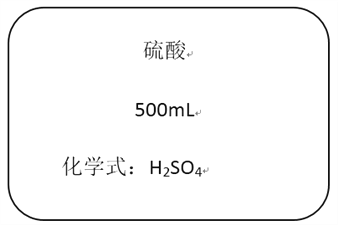
(1)取10mL该硫酸可配制成9.8%的硫酸____________________g。
(2)取适量该硫酸与锌反应可生成S02气体:Zn+2H2SO4 (浓)=ZnSO4+SO2↑+2H2O。反应一段时间后,还可能生成另一种气体,请解释其原因。_______________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小华想测定Cu—Zn合金中铜的质量分数,实验室只提供了一瓶稀盐酸和相关的仪器。为了测定该合金的组成,小华称取10克该合金粉末,在粉末中连续三次加入稀盐酸反应。每加一次盐酸,小华记录所得气体的质量,实验数据如下:
第一次 | 第二次 | 第三次 | |
连续加入盐酸的体积(ml) | 10 | 10 | 10 |
生成氢气的质量(g) | 0.08 | 0.08 | 0.04 |
(1)从上表数据分析,小华用10克合金粉末总共收集到___________克氢气。
(2)求出该合金中铜的质量分数为_________。(提示:Cu不与稀盐酸反应,锌与稀盐酸反应的化学方程式为Zn+2HCl=ZnCl2+H2↑)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据下图所示的实验过程和提供的数据计算:
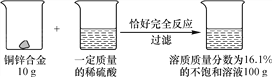
(1)最终生成的不饱和溶液中溶质的质量为________。
(2)合金中铜的质量分数________。
(3)求所加稀硫酸的溶质质量分数是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com