
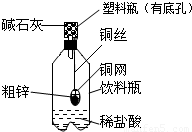
 某化学兴趣小组拟用如图装置对某粗锌样品进行纯度检测.请填写以下实验报告.
某化学兴趣小组拟用如图装置对某粗锌样品进行纯度检测.请填写以下实验报告.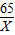 =
=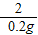 ,得:X=6.5g
,得:X=6.5g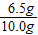 ×100%═65%.
×100%═65%.

 小夫子全能检测系列答案
小夫子全能检测系列答案科目:初中化学 来源: 题型:
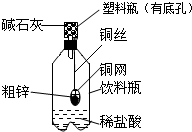 某化学兴趣小组拟用如图装置对某粗锌样品进行纯度检测.请填写以下实验报告.
某化学兴趣小组拟用如图装置对某粗锌样品进行纯度检测.请填写以下实验报告.查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| ||
| 2mw |
| 21 |
| m(1-w) |
| 20 |
| 2mw |
| 21 |
| m(1-w) |
| 20 |
| 2mw |
| 21 |
| m(1-w) |
| 20 |
| 2mw |
| 21 |
| m(1-w) |
| 20 |
查看答案和解析>>
科目:初中化学 来源:2013年初中毕业升学考试(湖南衡阳卷)化学(解析版) 题型:计算题
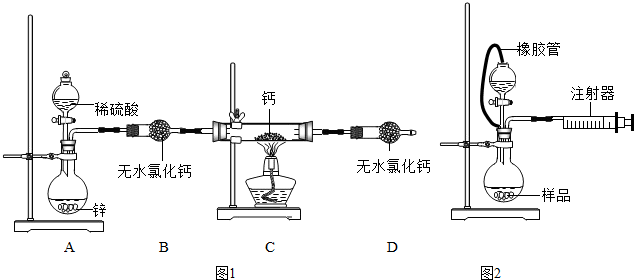
氢化钙(CaH2)固体是登山队员常用的能源提供剂.某化学兴趣小组拟用如图1所示的装置制备氢化钙,其反应的化学方程式为:Ca+H2 CaH2.
CaH2.
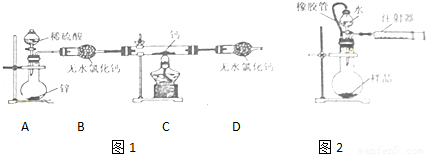
(1)CaH2中钙和氢元素的化合价分别为 ,装置中的无水氯化钙干燥装置也可用 来代替.
(2)利用该装置进行实验,步骤如下:检查装置的气密性后装入药品,打开分液漏斗活塞: (请按正确的顺序填入下列步骤的序号).
①加热反应一段时间 ②收集气体并检验其纯度 ③关闭分液漏斗活塞 ④停止加热,充分冷却
(3)为了确认进入装置C的氢气已经干燥,应在B、C之间再连接一装置X,装置X中加入的试剂是 .若氢气未充分干燥,装置X中的现象为 .
(4)为了测量上述实验中制得的氢化钙的纯度,该小组称取mg所制得样品,按如图2所示装置进行测定.旋开分液漏斗活塞,反应结束后充分冷却,注射器活塞由反应前的V1mL刻度处变化到V2mL刻度处(V2<V1,气体密度为dg/mL)
①橡胶管的作用为:a. ;b. .
②旋开分液漏斗活塞后,除发生CaH2+H2O═Ca(OH)2+H2↑的反应外,还最有可能发生的反应为 .
③用w表示氢化钙的纯度,请用一个等式表示出d、V1、V2和w之间的关系 .
④该小组乙同学认为去掉连接的注射器,也要计算出氢化钙的纯度.他同样称取mg样品,加入烧瓶中后称取反应前的质量为m1g,反应后的质量为m2g.乙同学表示出的m,m1,m2和w之间的关系的等式为 .
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
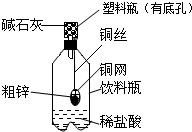 某化学兴趣小组拟用如图装置对某粗锌样品进行纯度检测.请填写以下实验报告.
某化学兴趣小组拟用如图装置对某粗锌样品进行纯度检测.请填写以下实验报告.查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
氢化钙(CaH2)固体是登山队员常用的能源提供剂.某化学兴趣小组拟用如图1所示的装置制备氢化钙,其反应的化学方程式为:Ca+H2 CaH2.
CaH2.
(1)CaH2中钙和氢元素的化合价分别为 ,装置中的无水氯化钙干燥装置也可用 来代替.
(2)利用该装置进行实验,步骤如下:检查装置的气密性后装入药品,打开分液漏斗活塞: (请按正确的顺序填入下列步骤的序号).
①加热反应一段时间 ②收集气体并检验其纯度 ③关闭分液漏斗活塞 ④停止加热,充分冷却
(3)为了确认进入装置C的氢气已经干燥,应在B、C之间再连接一装置X,装置X中加入的试剂是 .若氢气未充分干燥,装置X中的现象为 .
(4)为了测量上述实验中制得的氢化钙的纯度,该小组称取mg所制得样品,按如图2所示装置进行测定.旋开分液漏斗活塞,反应结束后充分冷却,注射器活塞由反应前的V1mL刻度处变化到V2mL刻度处(V2<V1,气体密度为dg/mL)
①橡胶管的作用为:a. ;b. .
②旋开分液漏斗活塞后,除发生CaH2+H2O═Ca(OH)2+H2↑的反应外,还最有可能发生的反应为 .
③用w表示氢化钙的纯度,请用一个等式表示出d、V1、V2和w之间的关系 .
④该小组乙同学认为去掉连接的注射器,也要计算出氢化钙的纯度.他同样称取mg样品,加入烧瓶中后称取反应前的质量为m1g,反应后的质量为m2g.乙同学表示出的m,m1,m2和w之间的关系的等式为 .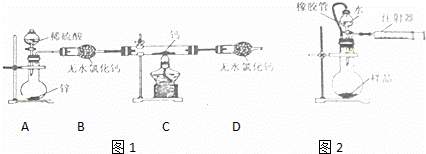
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com