
分析 促进可燃物燃烧的方法有:增大可燃物与氧气的接触面积或增大氧气的浓度,据此进行分析解答.
由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式.
成语“釜底抽薪”,含义是抽去锅底下的柴火,进行分析解答.
解答 解:煤块燃烧时,将煤块粉碎成煤粉是为了使煤与空气充分接触,利于煤充分燃烧.
由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式2CaCO3+O2+2SO2=2CaSO4+2X,反应前钙、碳、氧、硫原子个数分别为2、2、12、2,反应后的生成物中钙、碳、氧、硫原子个数分别为2、0、8、2,根据反应前后原子种类、数目不变,则2X分子中含2个碳原子和4个氧原子,则每个X分子由1个碳原子和2个氧原子构成,则物质X的化学式为CO2.
成语“釜底抽薪”,含义是抽去锅底下的柴火,清除了可燃物,达到灭火的目的.
故答案为:增大煤与氧气的接触面积,促进煤的燃烧;CO2;清除可燃物.
点评 本题难度不大,掌握促进可燃物燃烧的方法、化学反应前后原子守恒、灭火的原理等是正确解答本题的关键.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
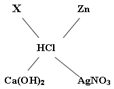 小政同学在复习盐酸化学性质时,归纳出了盐酸与其它物质间相互反应的关系图(图中“--”表示相连的两种物质能发生反应).
小政同学在复习盐酸化学性质时,归纳出了盐酸与其它物质间相互反应的关系图(图中“--”表示相连的两种物质能发生反应).查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
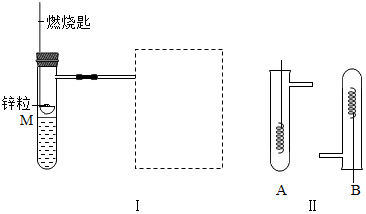 如图Ⅰ是实验室“制取氢气并还原氧化铜实验”的简易装置,其中铜制燃烧匙可以在试管M中上下移动,虚线框中的装置需从图Ⅱ中选取.图Ⅱ中的细铜丝一端绕成螺旋状,先在酒精灯火焰上加热,变黑后再迅速地伸到制得的氢气中.请回答下列问题:
如图Ⅰ是实验室“制取氢气并还原氧化铜实验”的简易装置,其中铜制燃烧匙可以在试管M中上下移动,虚线框中的装置需从图Ⅱ中选取.图Ⅱ中的细铜丝一端绕成螺旋状,先在酒精灯火焰上加热,变黑后再迅速地伸到制得的氢气中.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
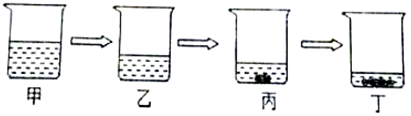
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com