
初中化学课上,同学们利用下列实验探究碱的化学性质: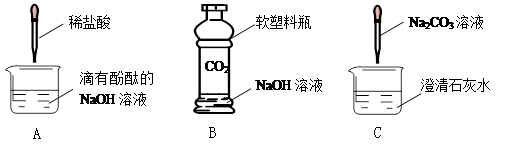
1)A实验中观察到的现象为 ,原因是(用化学方程式表示) 。
2)B实验中反应的化学方程式为 。
3)C实验中观察到的现象是 。
4)实验结束后,同学们将废液倒入同一只废液缸中,最后发现废液浑浊并显红色。
【提出问题】 废液中含有什么物质?
【假设猜想】 通过分析上述实验,同学们猜想:废液中除酚酞、碳酸钙及水以外一定含有 。
老师问:废液中还可能有什么物质?引发同学们热烈讨论,下面是大家的发言:
| 学生甲 | 可能有Ca(OH)2、NaOH | 学生丙 | 可能有Ca(OH)2、CaCl2 |
| 学生乙 | 可能有NaOH、Na2CO3 | 学生丁 | 可能有Na2CO3 |
| 学生戊 | 可能有NaOH | …… | ………… |
1)溶液红色逐渐褪去, HCl + NaOH = NaCl + H2O
2)CO2 + 2NaOH = Na2CO3 + H2O
3)有白色浑浊生成(或白色沉淀生成)
4)【猜想】NaCl
【结论】Na2CO3 , CaCl2、Ca(OH)2、NaOH
解析试题分析:1)氢氧化钠溶液呈碱性,可使酚酞变红。当加入稀盐酸后,二者发生中和反应。随着稀盐酸的加入,溶液的碱性会逐渐减弱至中性或酸性。观察的现象是:溶液红色会逐渐褪去。反应的化学方程式为:HCl + NaOH = NaCl + H2O
2)B中的二氧化碳会与氢氧化钠反应生成碳酸盐和水,反应的化学方程式为:CO2 + 2NaOH = Na2CO3 + H2O
3)石灰水是氢氧化钙的水溶液,会与碳酸钠反应生成白色的难溶于水的碳酸钙和水。所以反应的现象为:有白色沉淀生成。
4)【猜想】A中会生成氯化钠。且氯化钠不与后面的物质反应,因此一定存在。B中会生成碳酸钠。实验结束后,同学们将废液倒入同一只废液缸中,最后发现废液浑浊并显红色。说明C中的氢氧化钙有剩余,并与B中生成的碳酸钠反应生成碳酸钙沉淀而浑浊。由于碳酸钠参与了反应,所以它不一定存在,而是可能存在。显红色说明溶液呈碱性。在上述实验中呈碱性的有氢氧化钠、碳酸钠或氢氧化钙。无法确定哪一种。如A中盐酸有剩余,则可能存在还有氯化钙。因此一定存在的是氯化钠。
【结论】取一定量的废液过滤,向滤液中逐滴加入氯化钡溶液,得到白色沉淀,红色褪去。说明溶液中存在的碱性物质能与氯化钡反应,所以应为碳酸钠。由氯化钙、氢氧化钙一定不存在。最终溶液为无色,可确定氢氧化钠也不存在。
考点:科学探究、酸碱盐间的反应、过量推断


科目:初中化学 来源: 题型:探究题
(8分)小林同学在做探究质量守恒定律实验时,称取2.4g镁条在点燃的条件下与充足的空气反应,其反应的化学方程式为______________________________.(2分)实验完毕后,称得所得固体的质量小于4.0g.
【提出问题】固体质量为什么会小于4.0g呢?是否发生了其他反应呢?
【查阅资料】镁在空气中燃烧时,除了镁与氧气反应外,还可发生反应:
①2Mg+CO2点燃C+2MgO ② 3Mg+N2点燃Mg3N2
【猜想与假设】反应后固体质量小于4.0g是由于发生反应_______(填“①”或“②”)造成的,其理由是_____________________________.(2分)
【实验探究】根据初中化学所学知识用图所示装置除去空气中的氧气得到氮气(含少量稀有气体).可燃物应选择的物质是_________(填写物质的字母代号).
A.木炭 B.红磷 C.硫粉
选择的理由是________________________________________;
将点燃的镁条伸入所制得的氮气中,镁条在氮气中剧烈燃烧.
【实验结论】2.4g镁在空气中完全反应后所得固体质量小于4.0g,是由于生成的产物是___________的混合物所致.
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
某化学兴趣小组在做完制取二氧化碳的实验后(用石灰石与稀盐酸制取),对反应后反应器中剩余溶液的溶质成分产生了兴趣。他们继续进行了如下实验探究。
【分析推断】根据制取二氧化碳的反应原理,可以确定剩余溶液中一定含有氯化钙,但其中是否含有氯化氢需要通过实验来证明。若剩余溶液显酸性(含有
H+),说明含有氯化氢。
【查阅资料】碳酸钙不溶于水,氯化钙溶液不显酸性。
【实验过程】
将剩余溶液倒入烧杯中,微热后冷却至室温。
| | 实验操作 | 实验现象 | 实验结论 |
| 甲同学 | 取烧杯中溶液少许于试管中,向其中滴加 | 现象:溶液变为红色 | 溶液显酸性(含有H+),溶质中有氯化氢 |
| 乙同学 | 取烧杯中溶液少许于试管中,向其中加入少量锌粒 | 现象: 反应的化学方程式是: | |
| 丙同学 | 取烧杯中溶液少许于试管中,向其中加入少量石灰石 | 现象: |
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
小芳同学从超市购买了一瓶维生素C泡腾片。下图是标签上的部分内容。
| 维生素C泡腾片 功能:补充人体维生素C,增强机体抵抗力 主要成分:维生素C 辅料成分:碳酸氢钠、氯化钠、酒石酸晶体、蔗糖、糖精钠、阿朴胡萝卜醛、橘味香精、橙味香精、维生素B 贮藏:低温、避光、防潮 |
| 实验步骤 | 实验现象 | 实验结论 |
| 将一片维生素C泡腾片放入水中,将产生的气体通入__ __________________ | | |
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
某研究性学习小组在研究家乡的水资源的污染和保护时,对本镇的长泰县合成氨厂旁边的井水进行检测:取井水样品进行加热或加入碱性洗衣粉振荡时,明显闻到从水里散发出一股与氨厂附近相似的刺激性气味。该研究性学习小组决定对井水进行探究:
【作出猜想】联想到所学的化学知识,小东猜想可能是氨厂排出的废水污染了井水。他猜想的依据是 。
【表达交流】请你根据上述信息帮助小东归纳合成氨厂排出污染物的化学性质:(1) ;(2) 。
【设计实验】为了验证猜想,小方设计了如下实验方案:
(1)从合成氨厂取来碳酸氢氨作为样品;(2)取适量样品放入玻璃杯中,加入井水充分溶解。将所得溶液分为2份;(3)一份加入碱性洗衣粉,搅拌后闻气味;另一份加热后闻气味。
【反思评价】小东的实验方案存在着问题,你认为应怎样改进? 。
【获得结论】小东通过改进后的实验,确认是氨厂排出的废水污染了井水。
【探究启示】若村民还需饮用该井水,请你提出一条简便的处理方法: 。
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
科学家提出工业生产回收利用空气中CO2的构想:把空气吹入饱和碳酸钠溶液中,溶液可吸收CO2生成碳酸氢钠;加热碳酸氢钠固体又分解放出CO2;在合成塔内CO2与氢气反应生成甲醇(CH3OH)和水。简要的生产流程如下图所示:
[资料卡片] 碳酸氢钠分解温度是270℃,碳酸钠在856℃熔化,但还未达到分解温度。
请回答下列问题:
(1)吸收池中发生了化合反应,化学方程式为 。
(2)回收利用空气中的CO2,降低大气中CO2浓度,有利于减缓 。
(3)合成塔中发生反应的化学方程式为 。
(4)该流程中能循环利用的物质是 (填化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
某同学设计如图所示的实验装置,进行一氧化碳还原氧化铜的实验。试回答: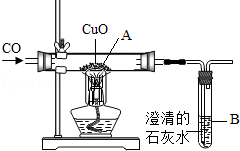
(1)该装置存在的一个主要问题是 :改进措施是 。[来源:学科(2)实验开始时,是先加热氧化铜,还是先通入一氧化碳? ,目的是为 。
(3)实验过程中,图中A处观察到的实验现象是 ;A处发生反应的化学方程式为 ;B处观察到的实验现象是 。
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
实验室常用加热(85℃)NH4Cl和NaNO2两种饱和溶液的方法制取N2,下图是实验室用这种方法制N2,并测定生成N2体积的装置(部分装置略去),请回答相关问题:
【查阅资料】:
1、NH4Cl和NaNO2反应生成NaCl、H2O及N2,并放出大量热量;
2、20℃时,NH4Cl的溶解度约为37g;
3、N2难溶于水,实验条件下,密度为1.25g·L—1。
【实验步骤】:
① ;
②20℃时,取0.78g饱和NH4Cl溶液放入烧瓶,连接装置;
③调节水准管,使其与量气管中液面相平,记录量气管中水面读数为12mL;
④打开分液漏斗活塞,逐滴滴入饱和NaNO2溶液,加热至反应发生,移走酒精灯;
⑤烧瓶中不再产生气泡时,关闭活塞;
⑥待冷却至室温,调节两边液面高度相平,记录量气管中水面读数为V mL;
⑦处理剩余药品,整理实验台。
【实验分析及数据处理】:
(1)写出装置中仪器的名称:a、 ;b、 ;
(2)反应的化学方程式为: ;
(3)完善实验步骤中的所缺部分:① ;
(4)步骤④中,移走酒精灯的目的是 ;
(5)NH4Cl是一种 (填“易溶”、“可溶”、“微溶”、“难溶”)物质。20℃时,其饱和溶液中溶质质量分数为 。根据实验数据计算,生成氮气约为多少毫升?(3分,计算过程中,中间数据保留2位小数,最终结果为整数;相对分子质量:Mr-NH4Cl:53.5、Mr-N2:28)
(6)根据计算结果,步骤⑥中V的数值为 ;
(7)实验中,实际测得氮气的体积偏大,可能原因是 。
A.实验中加入饱和NaNO2溶液的体积也被作为生成N2的体积
B.装置漏气
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
某同学欲探究市售 “双钙防蛀”牙膏、“皓清”牙膏和牙粉的主要成分。
【查阅资料】
(1)牙膏和牙粉均是由摩擦剂、活性剂、香料等成分构成。
(2)常用的摩擦剂有极细颗粒的碳酸钙(CaCO3) 和水合硅酸(SiO2·nH2O)等
(3)牙膏和牙粉中除了碳酸钙以外,其它物质均不与稀盐酸反应产生气体。
【实验一】探究“两种牙膏和牙粉中是否都含有碳酸钙?
| 步骤 | 实验操作 | 实验现象 |
| ① |  如图所示,取三只试管分别加入适量待测样品,再分别加入适量R 溶液。R 溶液是 。 | A试管中无明显变化, B和C试管中有无色气体生成。 |
| ② | 将B和C试管中生成的无色气体通入澄清石灰水。 | 现象Ⅱ: 。 |
| 步骤 | 实验操作 | 实验现象 |
| ① | 组装两套如图装置进行实验。分别取 (操作Ⅰ),放于锥形瓶中。并在分液漏斗中分别加入等质量的R 溶液。  | |
| ② | 打开分液漏斗注入一定量R 溶液,然后关闭活塞。 | 有气泡产生。 |
| ③ | 待②反应结束后,再打开分液漏斗,注入一定量R 溶液,然后关闭活塞。 | 无明显现象 |
| ④ | 称量反应后装置及药品的总质量并加以比较 | 加入“双钙防蛀”牙膏的装置及药品的总质量大于加入牙粉的装置及药品的总质量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com