
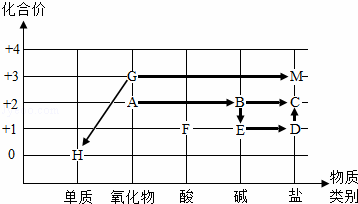
同学们依据物质类别和物质中某种元素的化合价构建了初中化学常见物质间的转化关系坐标图(图中“→”表示物质间的转化).
请回答下列问题:
(1)工业上可用化合反应来制备B,且反应时放出大量热,B的俗称为 .
(2)E的固体露置在空气中一段时间后质量会增加,其原因是 .
(3)H、G均可与F溶液反应,分别生成含该金属元素的两种盐溶液,则G与F溶液反应的化学方程式为 .
(4)在B溶液中加入一定量D溶液,过滤后取滤液,滴入过量F溶液,无明显现象,则滤液中的溶质是(写出所有可能) .
(5)已知金属铝可与E溶液反应生成偏铝酸钠(NaAlO2)和一种最轻的气体,写出该反应的化学方程式 .
(6)A~M九种物质中能与F溶液反应的物质有 种.
| 物质的相互转化和制备.. | |
| 专题: | 物质的制备. |
| 分析: | (1)根据生石灰溶于水放热分析 (2)根据氢氧化钠吸水性和与二氧化碳反应分析 (3)根据铁有亚铁盐和铁盐分析 (4)根据氢氧化钠与氢氧化钙的化学性质分析 (5)根据反应物生成物及书写方程式的原则书写方程式 (6)根据酸的化学性质分析 |
| 解答: | 解:(1)工业上可用化合反应来制备B,B是一种碱,且反应时放出大量热,在学过的物质中氧化钙与水化合生成氢氧化钙,放出大量的热,因此B为熟石灰或消石灰,A为氧化钙. (2)E是一种碱,露置在空气中一段时间后质量会增加,因此E是氢氧化钠,因其在空气中会吸水潮解,与二氧化碳反应生成碳酸钠而变质,故质量增加 (3)F是一种酸,H是单质,G是氧化物,HG都与酸反应生成含该金属元素的两种盐溶液,已知的元素中铁有+2和+3价,对应的盐有亚铁盐和铁盐,因此H是铁,G是氧化铁,G与F反应的化学方程式为Fe2O3+6HCl=2FeCl3+3H2O或Fe2O3+3H2SO4=Fe2(SO4)3+3H2O (4)B为氢氧化钙,在B溶液中加入D溶液产生沉淀,且D由氢氧化钠反应制取,因此D为碳酸钠,氢氧化钙与碳酸钠反应产生碳酸钙沉淀和氢氧化钠,过滤后取滤液,滴入过量的F(盐酸或硫酸)溶液无明显现象,说明碳酸钠没有剩余,氢氧化钙可能剩余,因此滤液中的溶质可能是氢氧化钠或氢氧化钠和氢氧化钙 (5)金属铝可与E(氢氧化钠)溶液反应生成偏铝酸钠(NaAlO2)和一种最轻的气体(氢气)化学方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑ (6)F是酸,A到M中能与酸发生反应的有A氧化钙,B氢氧化钙,C碳酸钙,D碳酸钠,E氢氧化钠,H 铁,G氧化铁七种 故答案为:(1)熟石灰或消石灰 (2)吸水潮解,与二氧化碳反应变质 (3)Fe2O3+6HCl=2FeCl3+3H2O或Fe2O3+3H2SO4=Fe2(SO4)3+3H2O (4)NaOH或NaOH和Ca(OH)2; (5)2Al+2NaOH+2H2O=2NaAlO2+3H2↑ (6)7 |
| 点评: | 要想解答好这类题目,首先,要理解和熟记物质的鉴别、推断及其方法,以及与之相关的知识.然后,根据所给的实验、问题情景或图表信息等,结合所学的相关知识和技能,以及自己的生产或生活经验所得,细致地分析题意等,并细心地探究、推理后,按照题目要求进行认真地选择或解答即可. |


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:初中化学 来源: 题型:
碱的化学性质是(写出有关的化学方程式)
( 1)碱溶液能与酸碱指示剂反应,使 试液变蓝,使 试液变红.
( 2)碱+非金属氧化物→ + .例:氢氧化钠和二氧化碳反应 氢氧化钙和二氧化碳反应 .
(3)碱+酸→ + .例:氢氧化钠和稀盐酸反应 氢氧化钙和稀硫酸反应 ,氢氧化钠和稀硫酸反应 .
查看答案和解析>>
科目:初中化学 来源: 题型:
用化学用语填空:
(1)地壳中含量最多的金属元素 ;
(2)空气中含量最多的气体 ;
(3)可用于气割、气焊的单质是 ;
(4)相对分子质量最小的氧化物 .
查看答案和解析>>
科目:初中化学 来源: 题型:
某品牌矿物质水标签的部分内容如图所示.
| 每100mL含量 (μg/100Ml) 氯化钾 70 硫酸镁 240 偏硅酸 180 pH(25℃):7.2﹣7.8 |
(1)氯化钾中氯离子的符号是 .
(2)硫酸镁中镁离子的结构示意图是 (填序号).
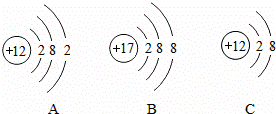
(3)25℃时,该矿物质水是 (填序号).
①酸性 ②中性 ③碱性.
查看答案和解析>>
科目:初中化学 来源: 题型:
关于分子和原子两种微粒的叙述正确的是
A.物质只能由分子构成 B.分子可分为原子,原子不可再分
C.相同原子可能构成不同分子 D.化学变化中分子数目一定发生变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com