
据报道,科学家在深海发现了一种外表象冰的固态物质,这种物质的成分是甲烷水合物(CH4•xH2O),称为可燃冰.测得这种晶体的结构为平均每46个水分子建8个笼,每个笼中容1个甲烷分子或1个游离的水分子则在这种晶体中共含 种分子.若每8个笼容有6个甲烷和2个水分子,则在这8个笼组成的整体中,甲烷与水的分子个数比是 .通常情况下,甲烷极难溶于水,也不与水发生反应,实验室用无水醋酸钠和碱石灰加热来制取,我们在实验室收集甲烷采用 ,原因是 .
| 有关化学式的计算和推断;常用气体的收集方法.. | |
| 专题: | 结合课本知识的信息. |
| 分析: | 根据题意,这种晶体的结构为平均每46个水分子建8个笼,每个笼中容1个甲烷分子或1个游离的水分子,进行分析解答. 考虑实验室选择气体收集方法时,是否能选用排水法要考虑气体的溶解性和是否与水反应;是否能选用排空气法要考虑气体的密度比空气大还是小;据此进行分析解答. |
| 解答: | 解:由题意,这种晶体的结构为平均每46个水分子建8个笼,每个笼中容1个甲烷分子或1个游离的水分子,即在这种晶体中共含2种分子; 若晶体中平均每46个H2O构建成8个笼,8个笼有6个容纳了CH4分子,另外2个笼被游离的H2O分子填充,因此晶体中有48个水分子,6个CH4分子.所以6CH4•48H2O即CH4•8H2O;甲烷与水的分子个数比是1:8. 甲烷极难溶于水,也不与水发生反应,我们在实验室收集甲烷采用排水法. 故答案为:2;1:8;排水法;难溶于水,也不与水发生反应. |
| 点评: | 本题难度不大,理解甲烷水合物微观构成的信息、收集方法要考虑气体的密度和溶解性是正确解答本题的关键. |


科目:初中化学 来源: 题型:
以下是某研究小组探究影响反应速率部分因素的相关实验数据.
| 实验序号 | 过氧化氢溶液浓度/% | 过氧化氢溶液体积/ml | 温度/C | 二氧化锰的用量/g | 收集氧气的体积/ml | 反应所需的时间/s |
| 1 | 5 | 1 | 20 | 0.1 | 4 | 16.74 |
| 2 | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
| 3 | 30 | 5 | 35 | 2 | 49.21 | |
| 4 | 30 | 5 | 55 | 2 | 10.76 |
(1)通过实验①和②对比可知,化学反应速率与 反应物浓度 有关;从实验③和④对比可知,化学反应速率与温度的关系是 .
(2)化学反应的实质是微观粒子相互接触、碰撞的结果,化学反应速率与微观粒子的概率有关.试从微观角度解释“反应物浓度越大,化学反应速率越快”的原因是 .
(3)用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,产生氧气的总质量 (选填“减小”或“不变”或“增大”).
查看答案和解析>>
科目:初中化学 来源: 题型:
现代客机外壳主要材料是铝锂合金,锂的原子结构示意图为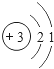 ,下列关于锂的说法错误的是( )
,下列关于锂的说法错误的是( )
|
| A. | 锂元素属于金属元素 | B. | 锂原子的质子数为3 |
|
| C. | 锂元素在化合物中通常是+3价 | D. | 锂原子在化学反应中容易失去电子 |
查看答案和解析>>
科目:初中化学 来源: 题型:
用数字和符号填空:
(1)三个氨气分子 .
(2)n个硫酸根离子 .
(3)标出氧化镁中镁元素的化合价 .
(4)海水中排在第三和第四位的元素组成的物质是 .
查看答案和解析>>
科目:初中化学 来源: 题型:
有X、Y、Z三种金属元素,把X和Y的单质分别放入稀硫酸中,Y溶解并有气体产生,X表面没有任何现象;Z的盐溶液不能用X制的容器盛装.根据以上事实判断,X、Y、Z的金属活动顺序为( )
|
| A. | Y>X>Z | B. | X>Y>Z | C. | Y>Z>X | D. | Z>Y>X |
查看答案和解析>>
科目:初中化学 来源: 题型:
小娟想测定黄铜样品(铜锌合金)中铜的质量分数.她取该合金的粉末20g,与足量的稀硫酸充分反应后,经测定产生了0.2g气体.请你帮助她算出该合金中铜的质量分数.
查看答案和解析>>
科目:初中化学 来源: 题型:
空气是我们赖以生存的物质,是一种宝贵的资源,请回答下列有关空气的问题:
(1)按 分数计算,空气中氧气约占 %
(2)空气中的氧气可以用于医疗急救,是由于氧气能 ;稀有气体是一种化学性质 的气体,试写出稀有气体的一种用途 .
(3)酥脆饼干放置在空气中久了会变软,是因为空气中有 (写物质名称);澄清的石灰水长期放置在空气中表面会有一层白膜,是因为空气中有 (写化学式)
(4)根据红磷燃烧测定空气中氧气含量的实验,请你推出氮气的一条物理性质 ;一条化学性质 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com